Actividad Práctica: Reconocimiento de Ácidos y Bases
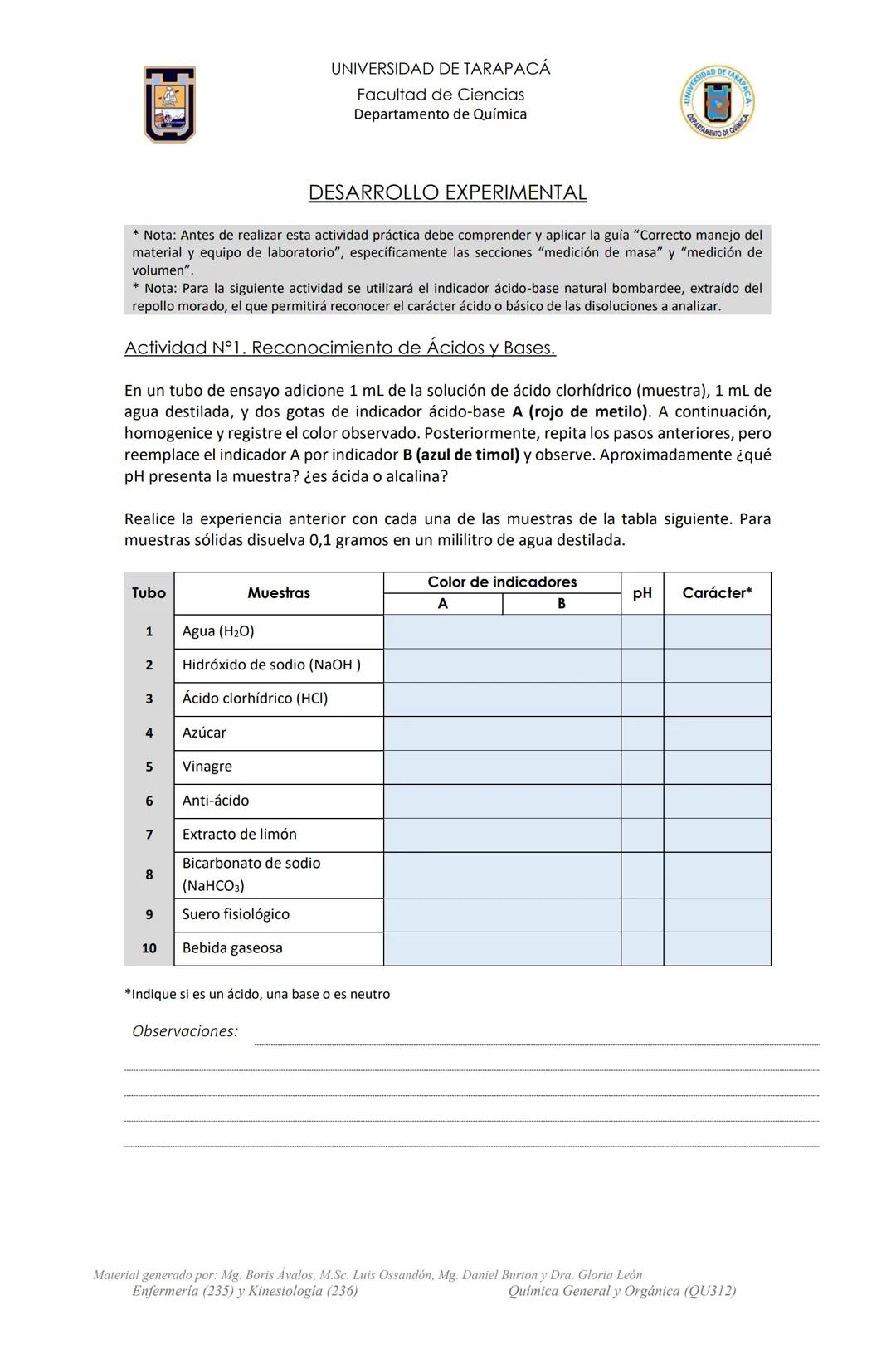
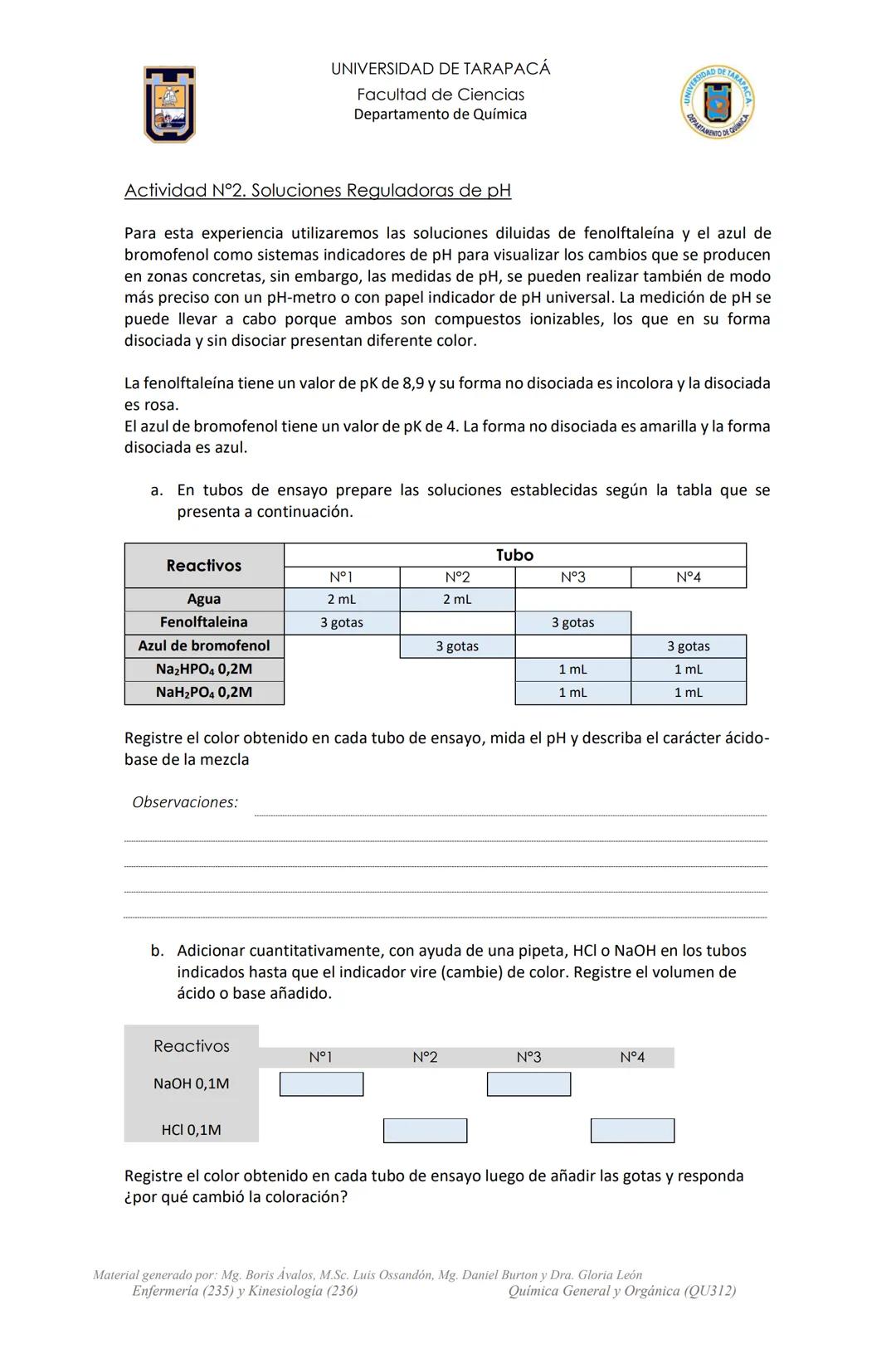
En esta práctica realizarás una actividad experimental para identificar el carácter ácido o básico de diferentes sustancias usando indicadores. Los indicadores ácido-base son compuestos que cambian de color dependiendo del pH de la solución, permitiéndonos clasificar las muestras.
Para esta actividad utilizarás dos indicadores:
- Indicador A: Rojo de metilo
- Indicador B: Azul de timol
- Adicionalmente, se usará bombardina, un indicador natural extraído del repollo morado
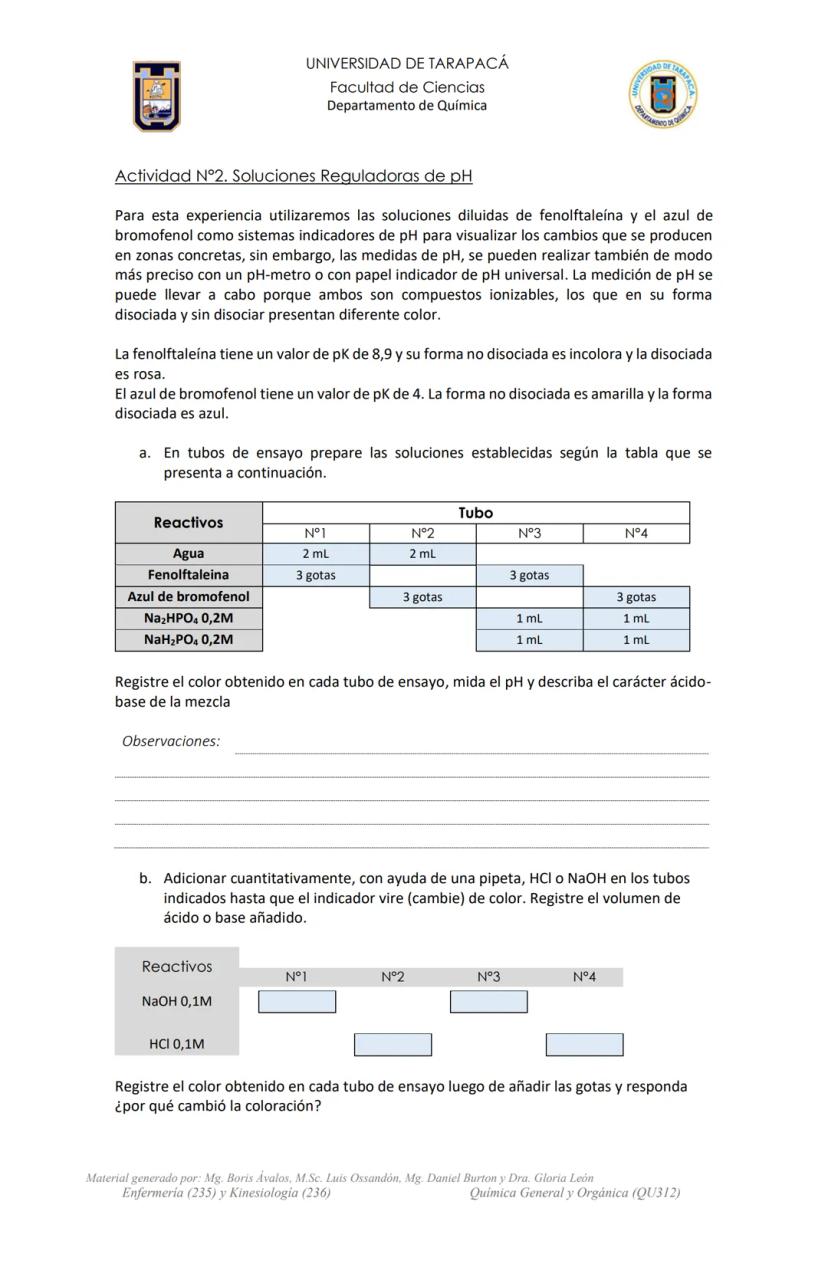
El procedimiento consiste en mezclar 1 mL de cada muestra con 1 mL de agua destilada y dos gotas del indicador, para luego observar el cambio de color. En caso de muestras sólidas, se disuelven 0,1 gramos en 1 mL de agua destilada.
Analizarás diversas sustancias cotidianas como agua, hidróxido de sodio (NaOH), ácido clorhídrico (HCl), azúcar, vinagre, antiácido, extracto de limón, bicarbonato de sodio (NaHCO₃), suero fisiológico y bebida gaseosa.
💡 Consejo práctico: Observa cuidadosamente los cambios de color y compáralos con una escala de pH para determinar con precisión si la muestra es ácida, neutra o básica.