Las reacciones químicas están presentes en todo nuestro entorno, desde... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
386
•
Actualizado Mar 23, 2026
•
agustin villegas
@agustinvillegas
Las reacciones químicas están presentes en todo nuestro entorno, desde... Mostrar más







¿Sabías que cada vez que enciendes un fósforo estás presenciando una reacción química? Las reacciones químicas son transformaciones donde los átomos se reorganizan, formando nuevas sustancias con propiedades diferentes.
Existen varios criterios para clasificar las reacciones químicas. El primer criterio se basa en la energía que interviene en el proceso. Algunas reacciones absorben energía (endergónicas) mientras que otras la liberan (exergónicas). Cuando esta energía es específicamente calor o luz, hablamos de reacciones endotérmicas o exotérmicas.
El segundo criterio considera las transformaciones moleculares que ocurren entre reactantes y productos. Según este criterio, las reacciones pueden ser de síntesis, descomposición o sustitución. La manera más fácil de identificar el tipo de reacción es analizando la ecuación química que la representa.
💡 ¡Dato clave! Una misma reacción puede clasificarse de varias maneras según diferentes criterios. Por ejemplo, la fotosíntesis es tanto endergónica como endotérmica.

En toda reacción química, además de la transformación de sustancias, ocurren intercambios energéticos. Estos intercambios suceden cuando se forman o rompen enlaces entre átomos.
Las reacciones exergónicas liberan energía durante el proceso, siendo la energía uno de los productos. Un ejemplo cotidiano es la respiración celular, donde la glucosa se combina con oxígeno produciendo dióxido de carbono, agua y energía química (ATP): C₆H₁₂O₆ + 6O₂ → 6CO₂ + 6H₂O + (Energía química)
Por otro lado, las reacciones endergónicas necesitan absorber energía para realizarse. La fotosíntesis es un ejemplo perfecto, pues requiere energía lumínica para convertir dióxido de carbono y agua en glucosa y oxígeno: 6CO₂ + 6H₂O + (Energía lumínica) → C₆H₁₂O₆ + 6O₂
Cuando la energía involucrada es específicamente calor o luz, usamos términos más específicos: reacciones exotérmicas (liberan calor) como la combustión, y reacciones endotérmicas (absorben calor) como la fotosíntesis. En las ecuaciones químicas, la energía térmica se suele representar con el símbolo Δ.
🔥 Recuerda: La energía en las reacciones exotérmicas aparece del lado de los productos, mientras que en las endotérmicas aparece del lado de los reactantes.

Cuando los átomos se reorganizan durante una reacción química, pueden formar distintas cantidades de productos a partir de los reactantes iniciales. Esta es otra forma muy útil de clasificar las reacciones.
Las reacciones de síntesis ocurren cuando dos o más sustancias simples se combinan para formar un único compuesto. Su estructura general es A + B → AB. Un ejemplo claro es la formación de óxido de magnesio: 2Mg + O₂ → 2MgO. Aquí, el magnesio se combina con oxígeno para formar un solo producto.
En contraste, las reacciones de descomposición suceden cuando un único reactante se descompone en dos o más productos más simples. Su estructura general es AB → A + B. Por ejemplo, cuando el óxido de mercurio (HgO) se calienta: 2HgO → 2Hg + O₂. En este tipo de reacciones, siempre tendremos más productos que reactantes.
🧪 Consejo práctico: Para identificar una reacción de síntesis o descomposición rápidamente, cuenta el número de reactantes y productos. En síntesis: varios reactantes → un producto; en descomposición: un reactante → varios productos.

Las reacciones de sustitución son fascinantes porque implican un intercambio de elementos entre los reactantes. En estas reacciones, el número de reactantes y productos es siempre el mismo.
En la sustitución simple, un elemento libre reemplaza a otro en un compuesto. Su esquema general es A + BC → AB + C. Un ejemplo cotidiano es cuando un metal reacciona con un ácido: Mg + 2HCl → MgCl₂ + H₂. Aquí, el magnesio reemplaza al hidrógeno en el ácido clorhídrico.
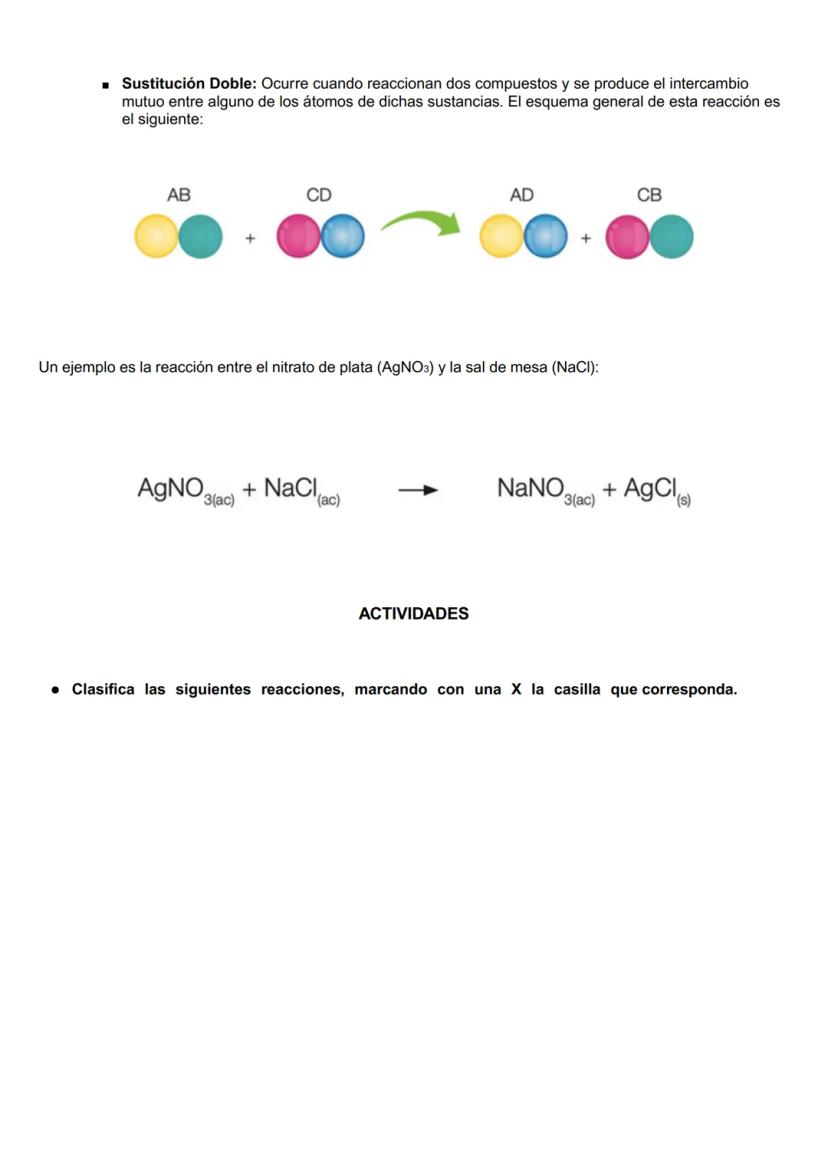
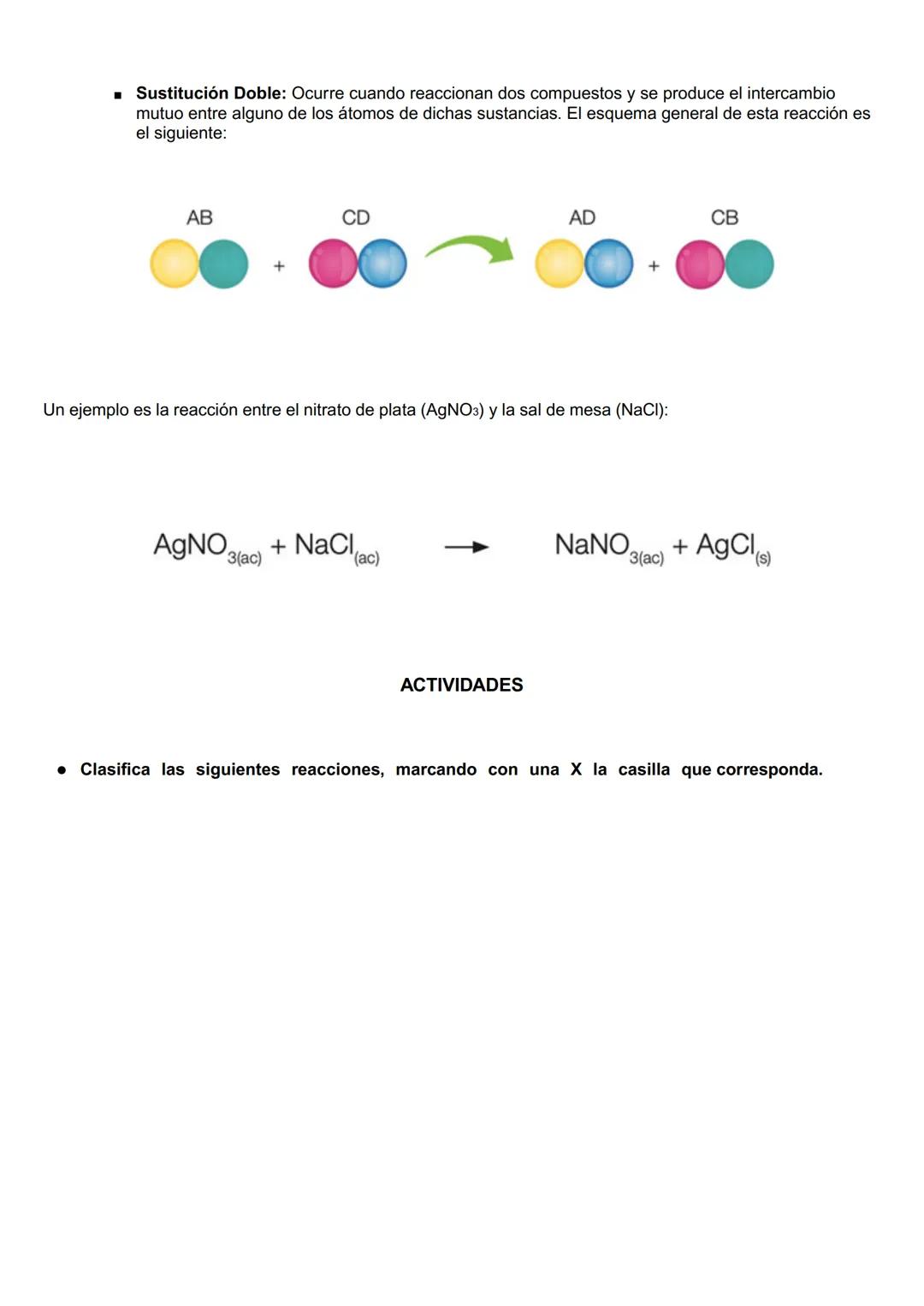
La sustitución doble ocurre cuando dos compuestos intercambian elementos entre sí. Su estructura general es AB + CD → AD + CB. Un ejemplo común es la reacción entre nitrato de plata y sal común: AgNO₃ + NaCl → NaNO₃ + AgCl. En este caso, los iones plata e hidrógeno intercambian sus posiciones.
Estas reacciones son muy importantes en la química de laboratorio y en muchos procesos industriales porque permiten obtener compuestos puros a partir de mezclas.
🔄 Truco para recordar: En sustitución simple, un elemento "soltero" desplaza a otro que está "en pareja". En sustitución doble, dos "parejas" intercambian sus "compañeros".
Ahora que conoces los distintos tipos de reacciones, es momento de poner en práctica estos conocimientos identificando ejemplos concretos.
Las reacciones de sustitución doble son comunes en soluciones acuosas, como cuando mezclamos soluciones de nitrato de plata y cloruro de sodio: AgNO₃ + NaCl → NaNO₃ + AgCl. El precipitado blanco de cloruro de plata que se forma es una evidencia visual de esta reacción.
Para clasificar correctamente una reacción química, observa cuidadosamente la ecuación. Fíjate en el número de reactantes y productos, si hay absorción o liberación de energía, y si hay intercambio de elementos. Por ejemplo, en 2H₂ + O₂ → 2H₂O tenemos una reacción de síntesis (varios reactantes forman un solo producto) y exotérmica (libera energía).
Es importante practicar con ejemplos variados para desarrollar la habilidad de identificar rápidamente los tipos de reacciones por su ecuación química.
📝 Estrategia de estudio: Crea fichas con diferentes ecuaciones químicas y practica clasificándolas. Luego, verifica tus respuestas y analiza por qué pertenecen a esa categoría específica.

Una forma efectiva de dominar la clasificación de reacciones es analizar ecuaciones químicas específicas. Veamos algunos ejemplos que te ayudarán a practicar:
La reacción 2H₂ + O₂ → 2H₂O es una reacción de síntesis porque dos sustancias simples (hidrógeno y oxígeno) se combinan para formar una sola sustancia (agua). También es exotérmica porque libera energía en forma de calor.
En cambio, CaCO₃ → CaO + CO₂ es una reacción de descomposición porque un compuesto se divide en dos sustancias más simples. Esta reacción es endotérmica porque necesita absorber calor para ocurrir.
Es útil también identificar las reacciones reversibles e irreversibles. Las reversibles pueden ocurrir en ambas direcciones dependiendo de las condiciones, mientras que las irreversibles solo ocurren en un sentido. Por ejemplo, la descomposición de CaCO₃ es reversible en condiciones adecuadas.
⚡ Recuerda: En las ecuaciones químicas, el símbolo "+" junto a los productos indica que la reacción es exotérmica, mientras que si está junto a los reactantes, la reacción es endotérmica.

Visualizar las reacciones químicas a nivel atómico nos ayuda enormemente a entender cómo ocurren las transformaciones. En los modelos moleculares, las esferas representan átomos o grupos de átomos.
Cuando observas un esquema donde dos tipos de moléculas reactantes producen una sola molécula más compleja, estás viendo una reacción de síntesis. Si una molécula se divide en varias más pequeñas, es una reacción de descomposición.
Para identificar reacciones de sustitución simple, busca esquemas donde un átomo libre reemplaza a otro dentro de una molécula. En la sustitución doble, verás dos moléculas intercambiando partes entre sí.
Estos modelos visuales son extremadamente útiles porque te permiten "ver" lo que sucede a nivel molecular, facilitando la comprensión de los procesos químicos que normalmente son invisibles.
🔍 Consejo visual: Cuando trabajes con modelos moleculares, fíjate en cómo los átomos cambian de "compañeros". Este simple enfoque te ayudará a identificar rápidamente el tipo de reacción que estás observando.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
agustin villegas
@agustinvillegas
Las reacciones químicas están presentes en todo nuestro entorno, desde la respiración celular hasta la combustión. Entender cómo clasificarlas nos ayuda a comprender mejor los procesos químicos que ocurren a diario. Esta guía te explicará los principales tipos de reacciones... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Sabías que cada vez que enciendes un fósforo estás presenciando una reacción química? Las reacciones químicas son transformaciones donde los átomos se reorganizan, formando nuevas sustancias con propiedades diferentes.
Existen varios criterios para clasificar las reacciones químicas. El primer criterio se basa en la energía que interviene en el proceso. Algunas reacciones absorben energía (endergónicas) mientras que otras la liberan (exergónicas). Cuando esta energía es específicamente calor o luz, hablamos de reacciones endotérmicas o exotérmicas.
El segundo criterio considera las transformaciones moleculares que ocurren entre reactantes y productos. Según este criterio, las reacciones pueden ser de síntesis, descomposición o sustitución. La manera más fácil de identificar el tipo de reacción es analizando la ecuación química que la representa.
💡 ¡Dato clave! Una misma reacción puede clasificarse de varias maneras según diferentes criterios. Por ejemplo, la fotosíntesis es tanto endergónica como endotérmica.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En toda reacción química, además de la transformación de sustancias, ocurren intercambios energéticos. Estos intercambios suceden cuando se forman o rompen enlaces entre átomos.
Las reacciones exergónicas liberan energía durante el proceso, siendo la energía uno de los productos. Un ejemplo cotidiano es la respiración celular, donde la glucosa se combina con oxígeno produciendo dióxido de carbono, agua y energía química (ATP): C₆H₁₂O₆ + 6O₂ → 6CO₂ + 6H₂O + (Energía química)
Por otro lado, las reacciones endergónicas necesitan absorber energía para realizarse. La fotosíntesis es un ejemplo perfecto, pues requiere energía lumínica para convertir dióxido de carbono y agua en glucosa y oxígeno: 6CO₂ + 6H₂O + (Energía lumínica) → C₆H₁₂O₆ + 6O₂
Cuando la energía involucrada es específicamente calor o luz, usamos términos más específicos: reacciones exotérmicas (liberan calor) como la combustión, y reacciones endotérmicas (absorben calor) como la fotosíntesis. En las ecuaciones químicas, la energía térmica se suele representar con el símbolo Δ.
🔥 Recuerda: La energía en las reacciones exotérmicas aparece del lado de los productos, mientras que en las endotérmicas aparece del lado de los reactantes.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Cuando los átomos se reorganizan durante una reacción química, pueden formar distintas cantidades de productos a partir de los reactantes iniciales. Esta es otra forma muy útil de clasificar las reacciones.
Las reacciones de síntesis ocurren cuando dos o más sustancias simples se combinan para formar un único compuesto. Su estructura general es A + B → AB. Un ejemplo claro es la formación de óxido de magnesio: 2Mg + O₂ → 2MgO. Aquí, el magnesio se combina con oxígeno para formar un solo producto.
En contraste, las reacciones de descomposición suceden cuando un único reactante se descompone en dos o más productos más simples. Su estructura general es AB → A + B. Por ejemplo, cuando el óxido de mercurio (HgO) se calienta: 2HgO → 2Hg + O₂. En este tipo de reacciones, siempre tendremos más productos que reactantes.
🧪 Consejo práctico: Para identificar una reacción de síntesis o descomposición rápidamente, cuenta el número de reactantes y productos. En síntesis: varios reactantes → un producto; en descomposición: un reactante → varios productos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las reacciones de sustitución son fascinantes porque implican un intercambio de elementos entre los reactantes. En estas reacciones, el número de reactantes y productos es siempre el mismo.
En la sustitución simple, un elemento libre reemplaza a otro en un compuesto. Su esquema general es A + BC → AB + C. Un ejemplo cotidiano es cuando un metal reacciona con un ácido: Mg + 2HCl → MgCl₂ + H₂. Aquí, el magnesio reemplaza al hidrógeno en el ácido clorhídrico.
La sustitución doble ocurre cuando dos compuestos intercambian elementos entre sí. Su estructura general es AB + CD → AD + CB. Un ejemplo común es la reacción entre nitrato de plata y sal común: AgNO₃ + NaCl → NaNO₃ + AgCl. En este caso, los iones plata e hidrógeno intercambian sus posiciones.
Estas reacciones son muy importantes en la química de laboratorio y en muchos procesos industriales porque permiten obtener compuestos puros a partir de mezclas.
🔄 Truco para recordar: En sustitución simple, un elemento "soltero" desplaza a otro que está "en pareja". En sustitución doble, dos "parejas" intercambian sus "compañeros".

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Ahora que conoces los distintos tipos de reacciones, es momento de poner en práctica estos conocimientos identificando ejemplos concretos.
Las reacciones de sustitución doble son comunes en soluciones acuosas, como cuando mezclamos soluciones de nitrato de plata y cloruro de sodio: AgNO₃ + NaCl → NaNO₃ + AgCl. El precipitado blanco de cloruro de plata que se forma es una evidencia visual de esta reacción.
Para clasificar correctamente una reacción química, observa cuidadosamente la ecuación. Fíjate en el número de reactantes y productos, si hay absorción o liberación de energía, y si hay intercambio de elementos. Por ejemplo, en 2H₂ + O₂ → 2H₂O tenemos una reacción de síntesis (varios reactantes forman un solo producto) y exotérmica (libera energía).
Es importante practicar con ejemplos variados para desarrollar la habilidad de identificar rápidamente los tipos de reacciones por su ecuación química.
📝 Estrategia de estudio: Crea fichas con diferentes ecuaciones químicas y practica clasificándolas. Luego, verifica tus respuestas y analiza por qué pertenecen a esa categoría específica.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Una forma efectiva de dominar la clasificación de reacciones es analizar ecuaciones químicas específicas. Veamos algunos ejemplos que te ayudarán a practicar:
La reacción 2H₂ + O₂ → 2H₂O es una reacción de síntesis porque dos sustancias simples (hidrógeno y oxígeno) se combinan para formar una sola sustancia (agua). También es exotérmica porque libera energía en forma de calor.
En cambio, CaCO₃ → CaO + CO₂ es una reacción de descomposición porque un compuesto se divide en dos sustancias más simples. Esta reacción es endotérmica porque necesita absorber calor para ocurrir.
Es útil también identificar las reacciones reversibles e irreversibles. Las reversibles pueden ocurrir en ambas direcciones dependiendo de las condiciones, mientras que las irreversibles solo ocurren en un sentido. Por ejemplo, la descomposición de CaCO₃ es reversible en condiciones adecuadas.
⚡ Recuerda: En las ecuaciones químicas, el símbolo "+" junto a los productos indica que la reacción es exotérmica, mientras que si está junto a los reactantes, la reacción es endotérmica.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Visualizar las reacciones químicas a nivel atómico nos ayuda enormemente a entender cómo ocurren las transformaciones. En los modelos moleculares, las esferas representan átomos o grupos de átomos.
Cuando observas un esquema donde dos tipos de moléculas reactantes producen una sola molécula más compleja, estás viendo una reacción de síntesis. Si una molécula se divide en varias más pequeñas, es una reacción de descomposición.
Para identificar reacciones de sustitución simple, busca esquemas donde un átomo libre reemplaza a otro dentro de una molécula. En la sustitución doble, verás dos moléculas intercambiando partes entre sí.
Estos modelos visuales son extremadamente útiles porque te permiten "ver" lo que sucede a nivel molecular, facilitando la comprensión de los procesos químicos que normalmente son invisibles.
🔍 Consejo visual: Cuando trabajes con modelos moleculares, fíjate en cómo los átomos cambian de "compañeros". Este simple enfoque te ayudará a identificar rápidamente el tipo de reacción que estás observando.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
2
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas de Estudio Interactivas ✓ Prueba Completa de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia