La teoría atómica es el fundamento científico que explica cómo... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
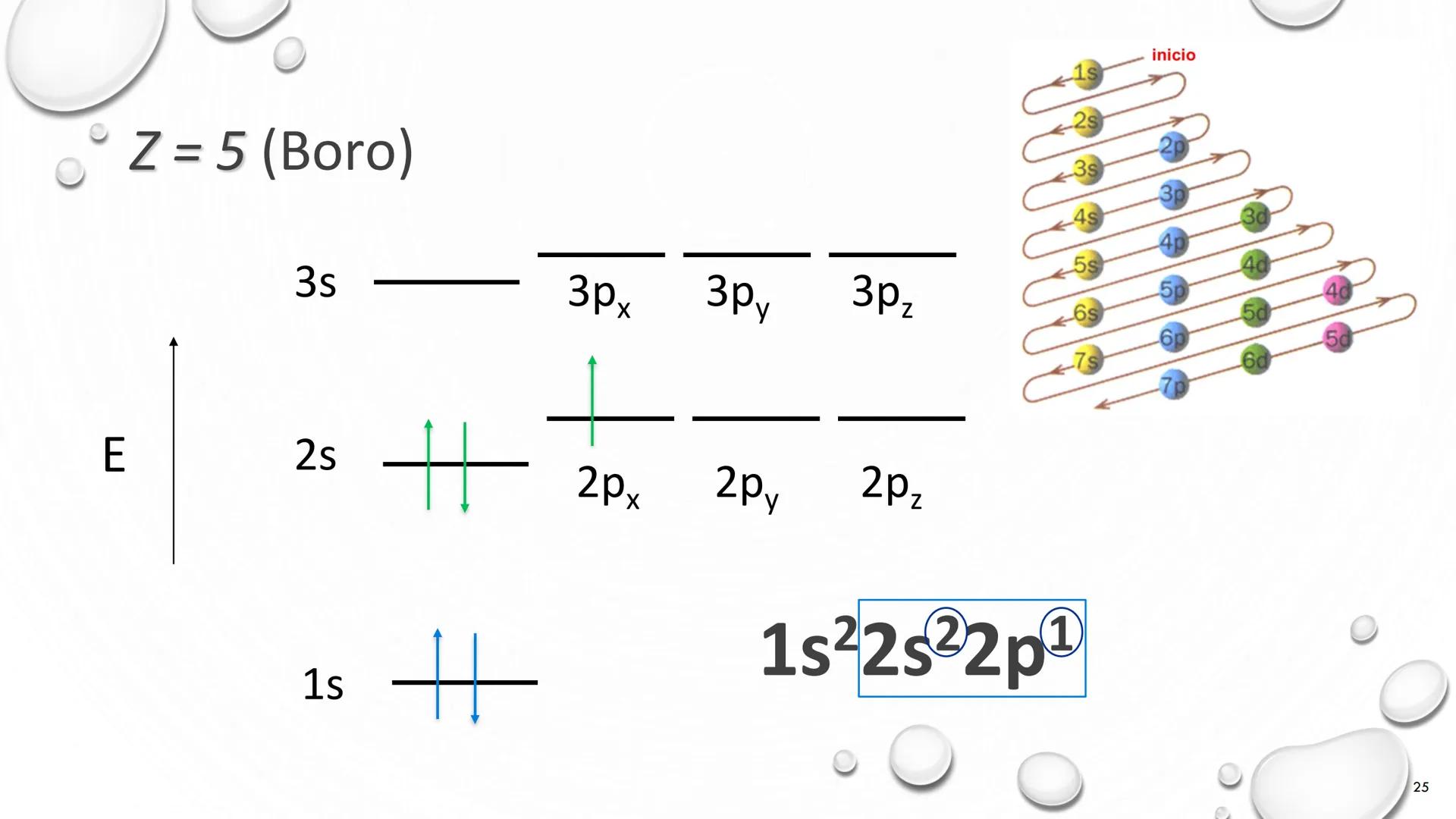
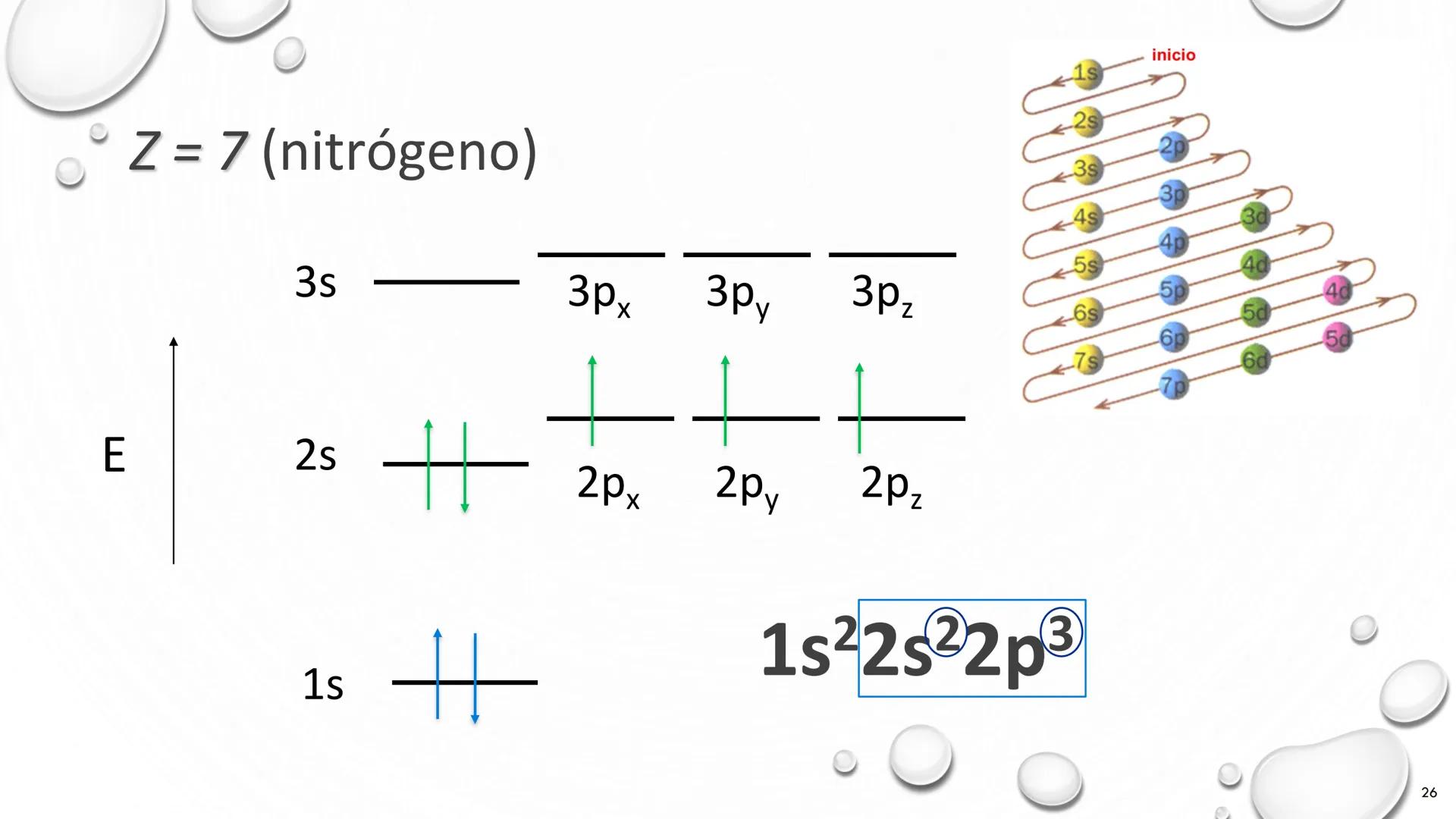
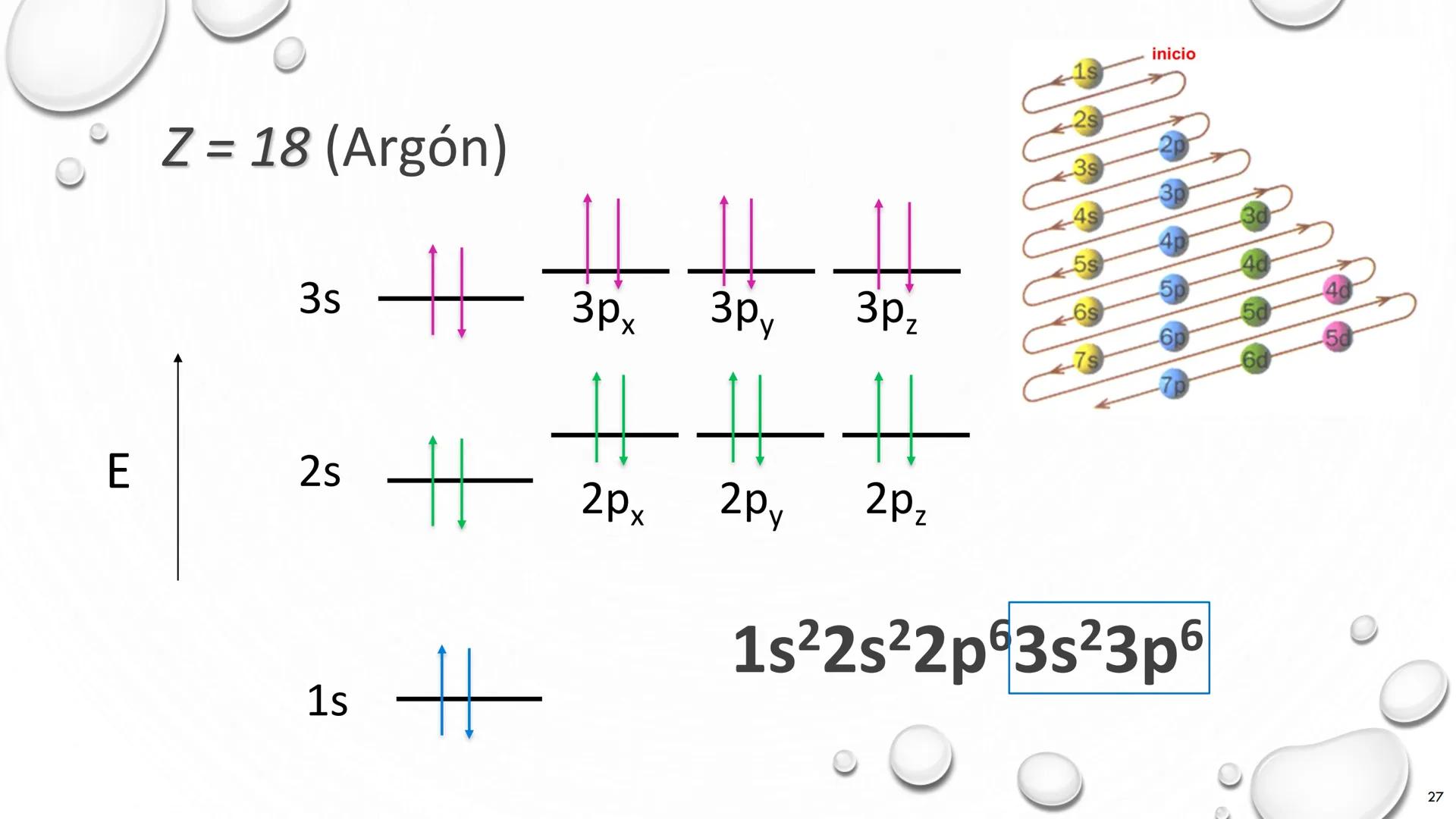
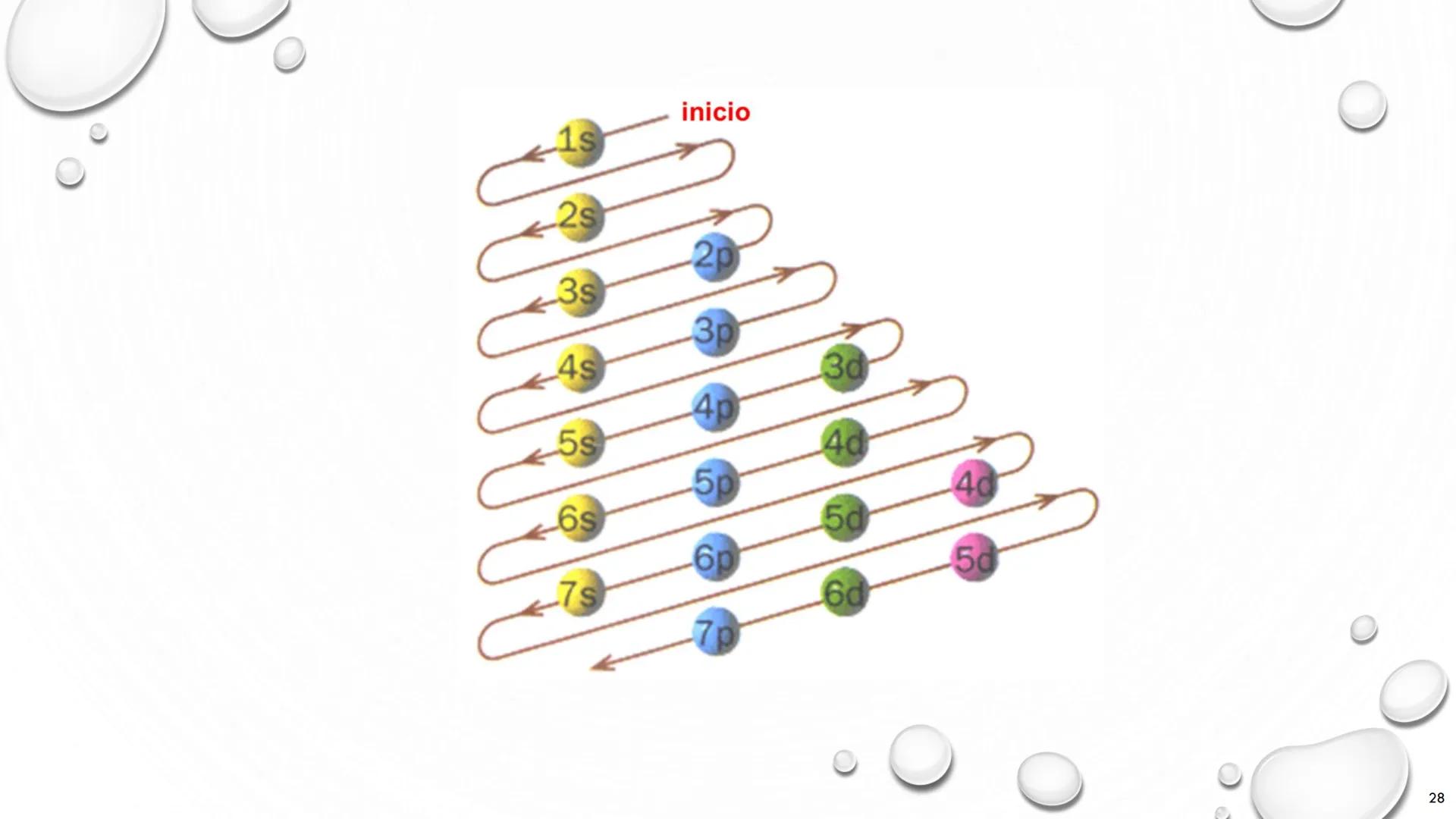
Molecular Electron Structure Representation
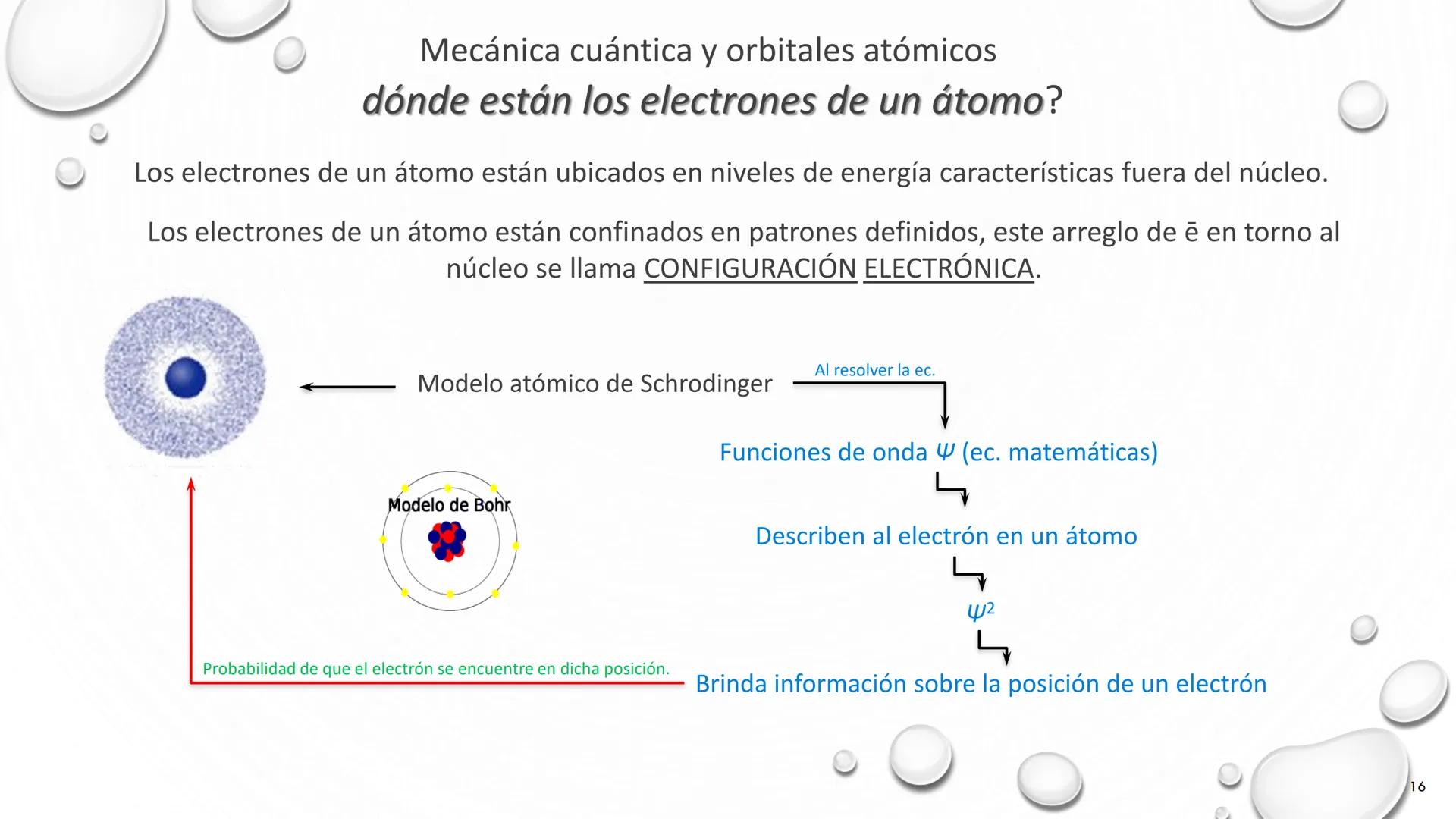
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
66
•
Actualizado Apr 6, 2026
•
_2ogj9
@_2ogj9
La teoría atómica es el fundamento científico que explica cómo... Mostrar más

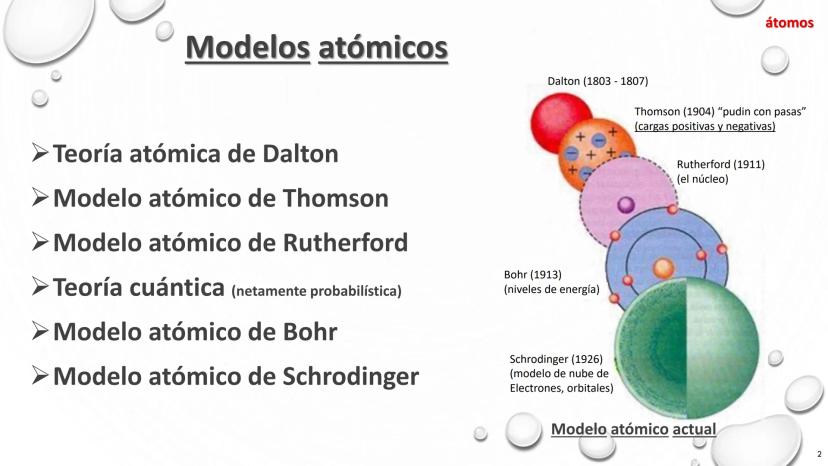




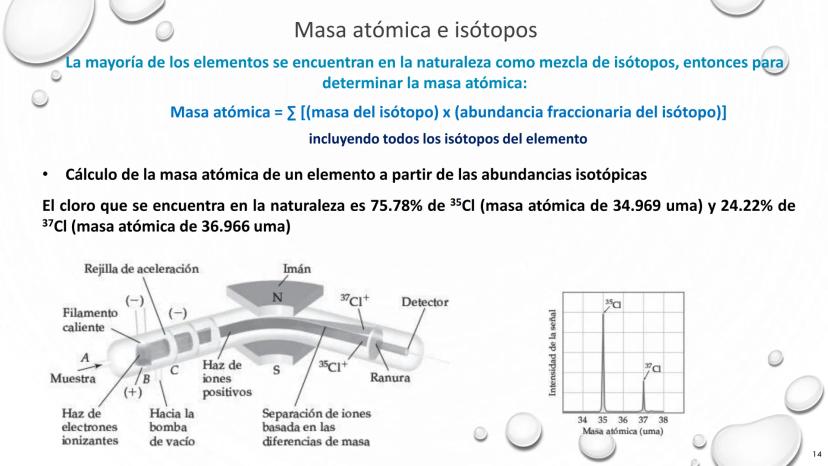
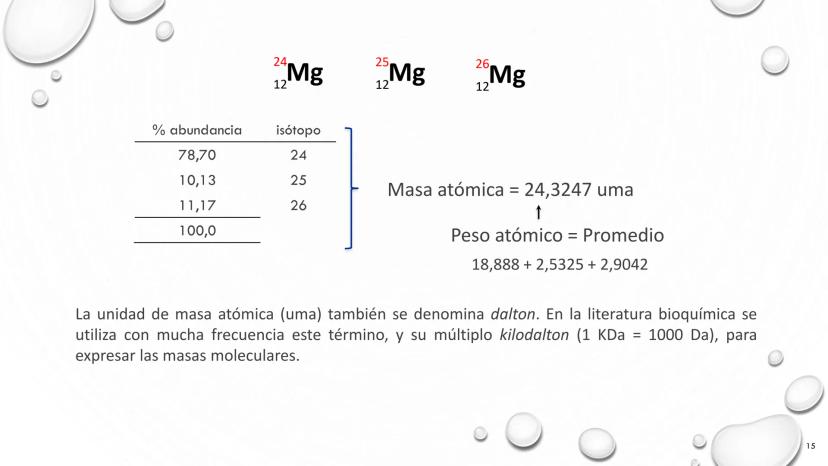
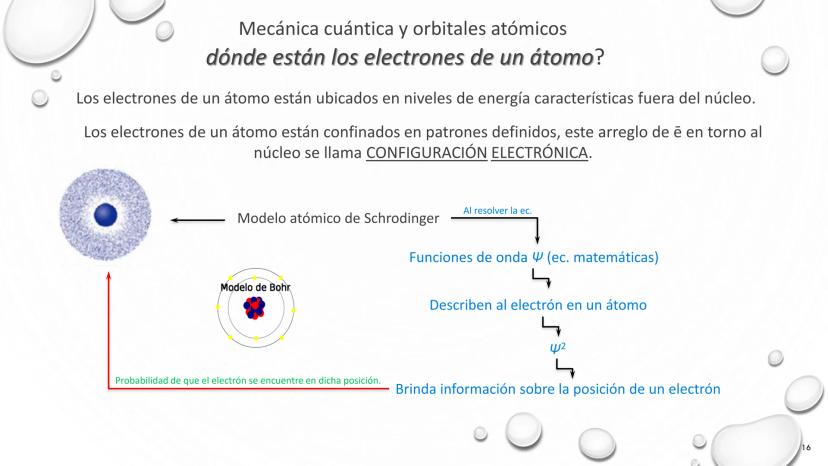

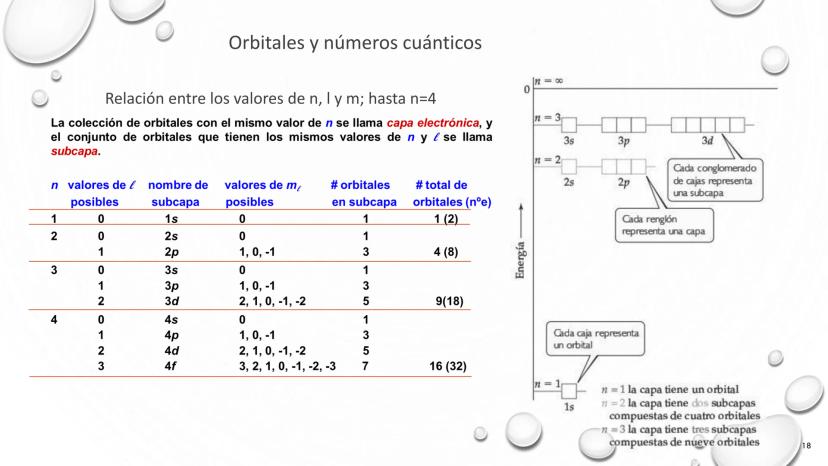
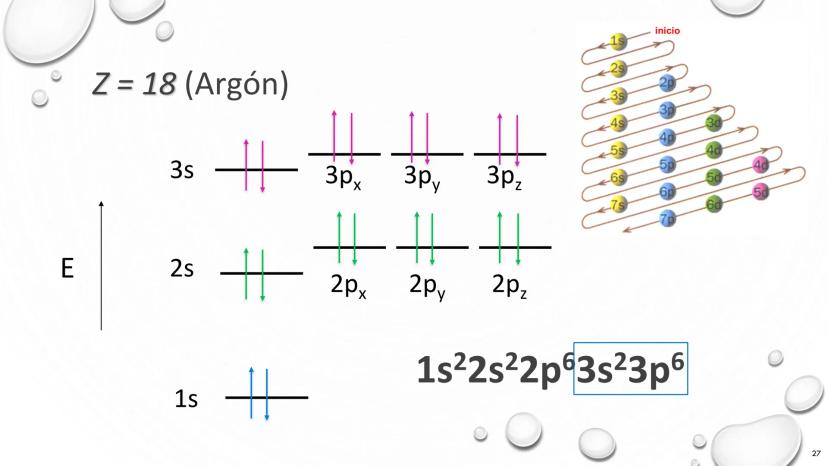
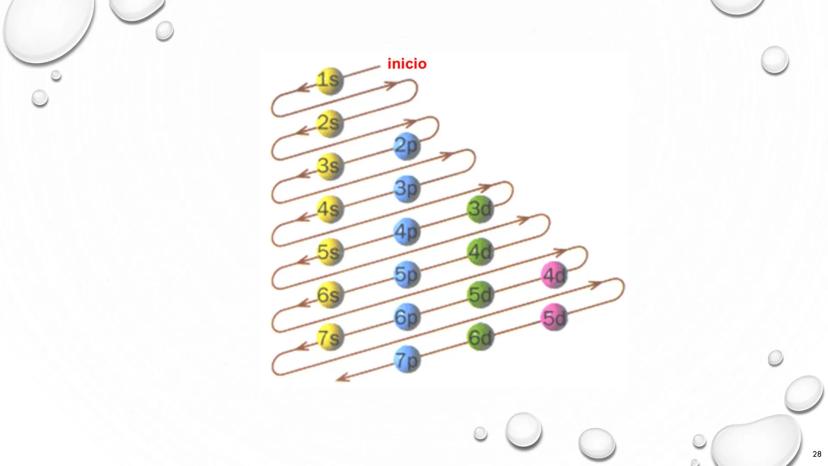


La comprensión del átomo ha evolucionado dramáticamente desde el siglo XIX hasta la actualidad. Esta línea de tiempo representa el desarrollo de los modelos atómicos, mostrando cómo nuestro entendimiento de la materia ha pasado por varias transformaciones fundamentales.
En 1803, Dalton propuso que toda materia está compuesta por partículas indivisibles. Para 1897, Thomson descubrió el electrón, cambiando completamente nuestra visión. Luego, en 1909, Rutherford identificó el núcleo atómico, y en 1913, Bohr introdujo la idea de niveles energéticos específicos para los electrones.
💡 Cada modelo atómico no simplemente reemplazó al anterior, sino que incorporó las observaciones anteriores y añadió nuevas capas de entendimiento sobre la estructura fundamental de la materia.
El modelo actual es el resultado de siglos de investigación científica y nos permite explicar prácticamente todos los fenómenos químicos y físicos relacionados con la materia.
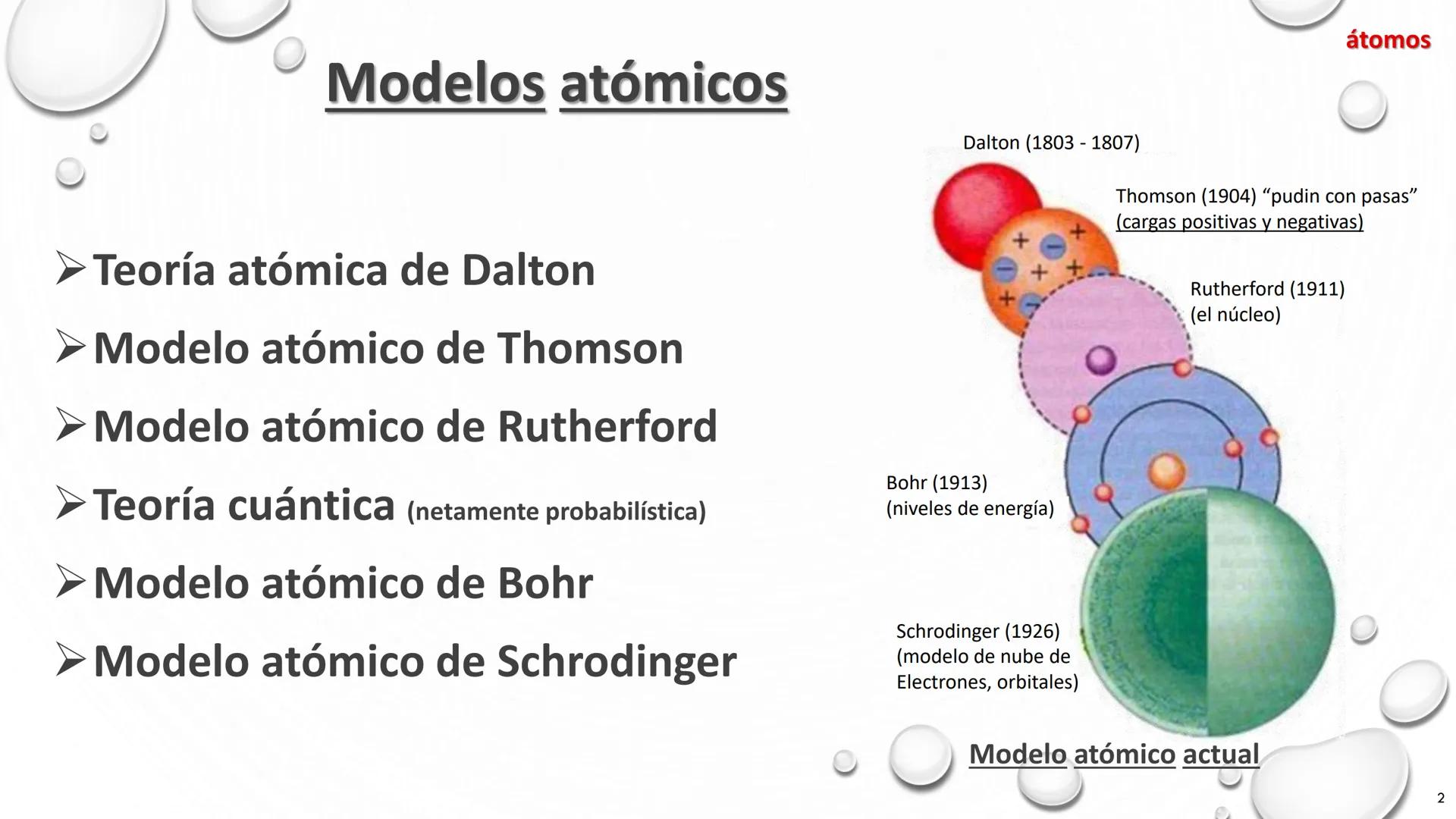
La evolución de los modelos atómicos representa uno de los mayores avances científicos. Cada modelo nos ha acercado a entender la verdadera naturaleza de la materia.
Dalton (1803-1807) propuso que todos los elementos están formados por átomos indivisibles, como pequeñas esferas sólidas. Este modelo simple sentó las bases para el desarrollo posterior.
Thomson (1904) propuso el modelo del "pudín con pasas", donde los electrones negativos estaban incrustados en una masa positiva, como pasas en un pudín.
Rutherford (1911) descubrió que el átomo tiene un núcleo central donde se concentra la carga positiva, con electrones girando alrededor, similar al sistema solar.
Bohr (1913) introdujo los niveles de energía, estableciendo que los electrones orbitan el núcleo en niveles fijos y específicos.
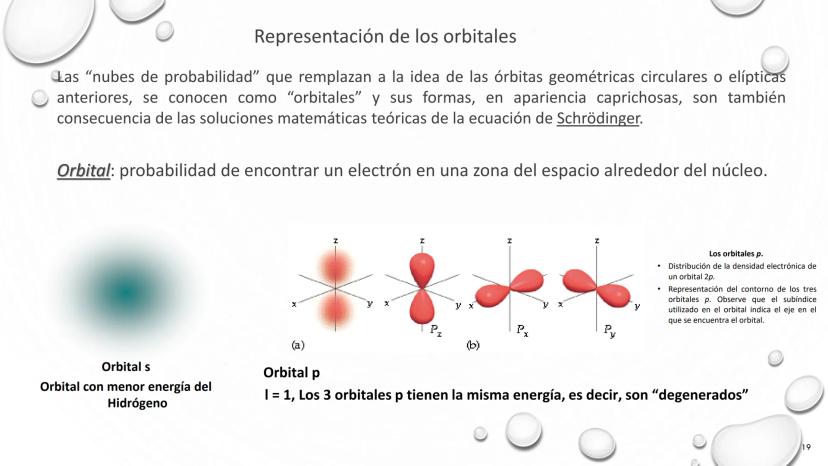
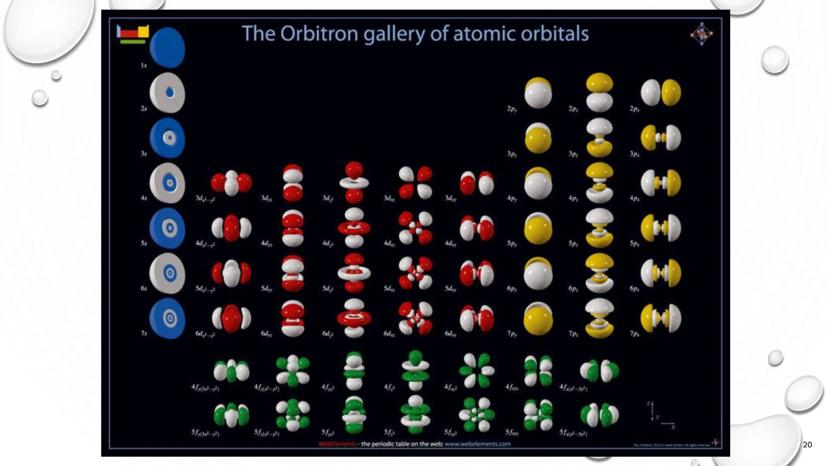
Schrödinger (1926) revolucionó nuestra comprensión con el modelo de nube de electrones y orbitales, basado en la mecánica cuántica y probabilidades.
El modelo atómico actual combina aspectos de todos los anteriores, pero se basa principalmente en la teoría cuántica, describiendo los electrones como nubes de probabilidad en lugar de partículas con posiciones exactas.
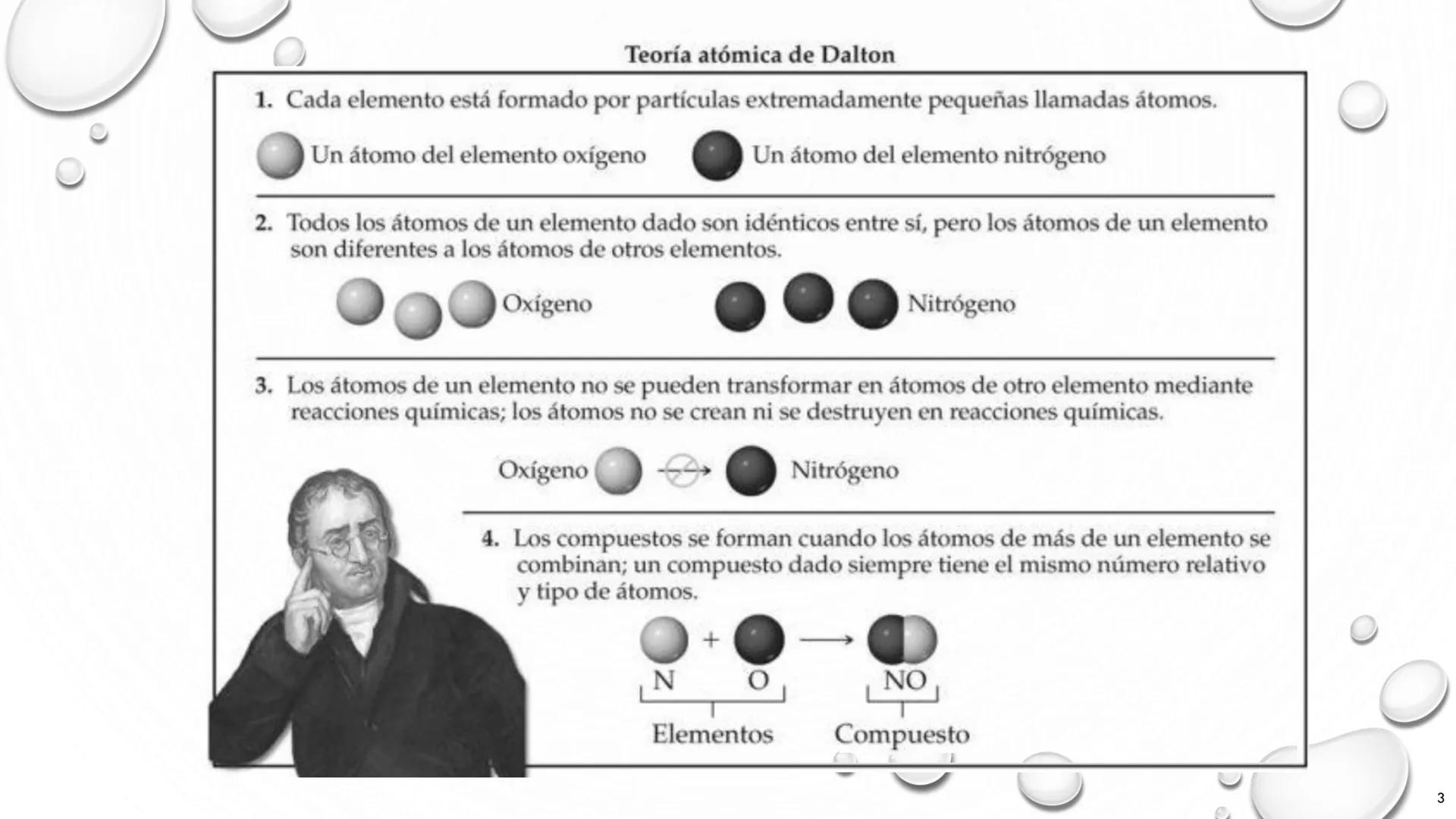
La teoría de Dalton (1803-1807) fue revolucionaria al proponer que toda materia está formada por unidades fundamentales indivisibles. Sus cuatro postulados principales siguen siendo relevantes en la química básica.
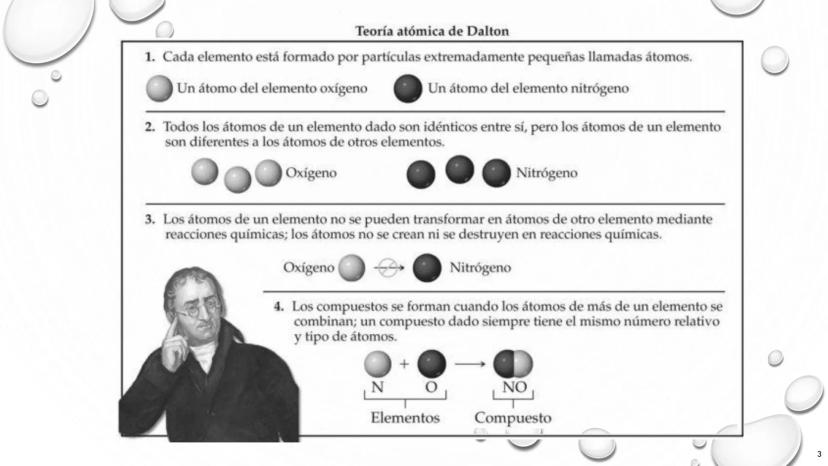
Los elementos están formados por partículas diminutas llamadas átomos. Estas partículas son tan pequeñas que no podían verse con la tecnología de la época, pero Dalton dedujo su existencia mediante observaciones indirectas.
Los átomos de un mismo elemento son idénticos entre sí, pero diferentes a los de otros elementos. Por ejemplo, todos los átomos de oxígeno son iguales entre sí, pero distintos a los átomos de nitrógeno.
Los átomos son indestructibles y no se transforman durante las reacciones químicas. Este principio establece que los átomos no se crean ni se destruyen, solo se reorganizan.
Los compuestos se forman cuando átomos de diferentes elementos se combinan en proporciones fijas. Por ejemplo, el óxido nítrico (NO) siempre contiene un átomo de nitrógeno y uno de oxígeno.
🔍 Aunque algunos aspectos de la teoría de Dalton han sido modificados con el tiempo (ahora sabemos que los átomos son divisibles), sus ideas fundamentales sobre la conservación de la materia y las proporciones constantes siguen siendo pilares de la química moderna.
Esta teoría permitió explicar muchas observaciones experimentales y sentó las bases para el desarrollo de la química moderna.

La teoría atómica de Dalton no surgió de la nada, sino que explicaba elegantemente varias leyes químicas que ya habían sido observadas experimentalmente.
La ley de la composición constante afirma que un compuesto específico siempre contiene los mismos elementos en las mismas proporciones. Por ejemplo, el agua siempre tiene dos átomos de hidrógeno por cada átomo de oxígeno, independientemente de su origen.
La ley de conservación de la masa establece que la masa total antes y después de una reacción química permanece constante. Esto tiene sentido con la teoría de Dalton, ya que los átomos no se crean ni se destruyen, solo se reorganizan.
La ley de las proporciones múltiples dice que cuando dos elementos forman más de un compuesto, las masas de un elemento que se combinan con una masa fija del otro están en relación de números enteros pequeños. Esta ley fue crucial para demostrar la naturaleza atómica de la materia.
Estas leyes proporcionaron evidencia sólida para la teoría atómica, permitiendo a los científicos predecir el comportamiento químico incluso antes de poder observar directamente los átomos.
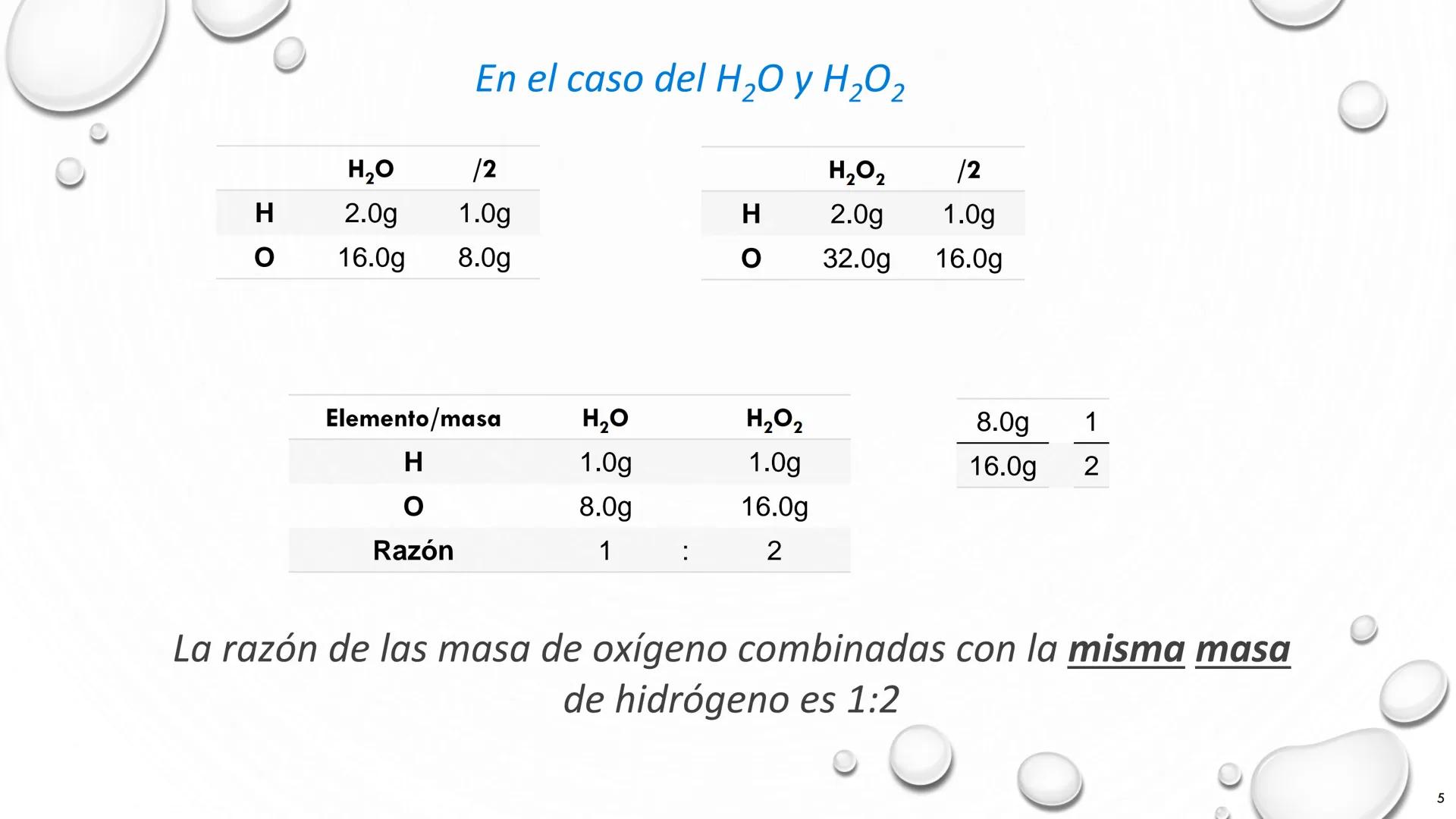
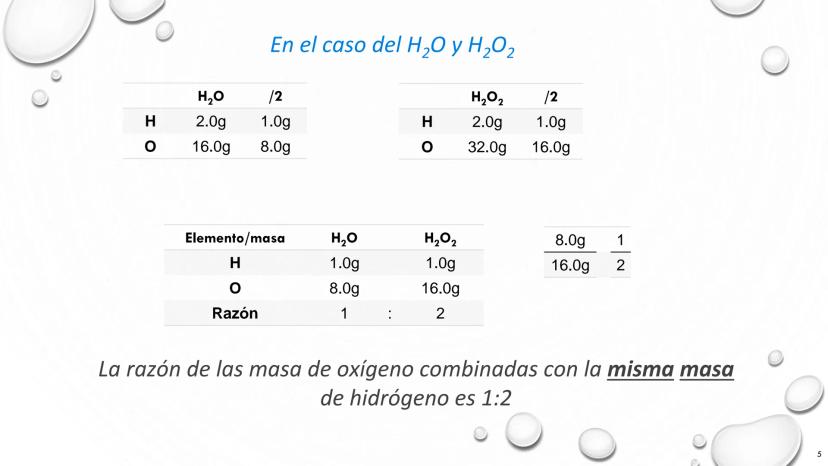
¿Te has preguntado cómo podemos demostrar la ley de las proporciones múltiples? El agua (H₂O) y el peróxido de hidrógeno (H₂O₂) nos ofrecen un ejemplo perfecto.
Ambos compuestos contienen los mismos elementos (hidrógeno y oxígeno), pero en proporciones diferentes. Al analizar 1 gramo de hidrógeno en cada compuesto:
| Elemento | H₂O | H₂O₂ |
|---|---|---|
| H | 1.0g | 1.0g |
| O | 8.0g | 16.0g |
La relación entre las masas de oxígeno es exactamente 1:2, un número entero simple. Este patrón no es coincidencia, sino evidencia directa de que la materia está compuesta por átomos que se combinan en proporciones fijas.
💡 La razón por la que obtenemos números enteros simples es porque estamos contando átomos, aunque indirectamente a través de sus masas.
Este fenómeno se observa constantemente en todos los compuestos químicos y proporciona una de las evidencias más convincentes de la naturaleza atómica de la materia, confirmando la brillante intuición de Dalton hace más de 200 años.
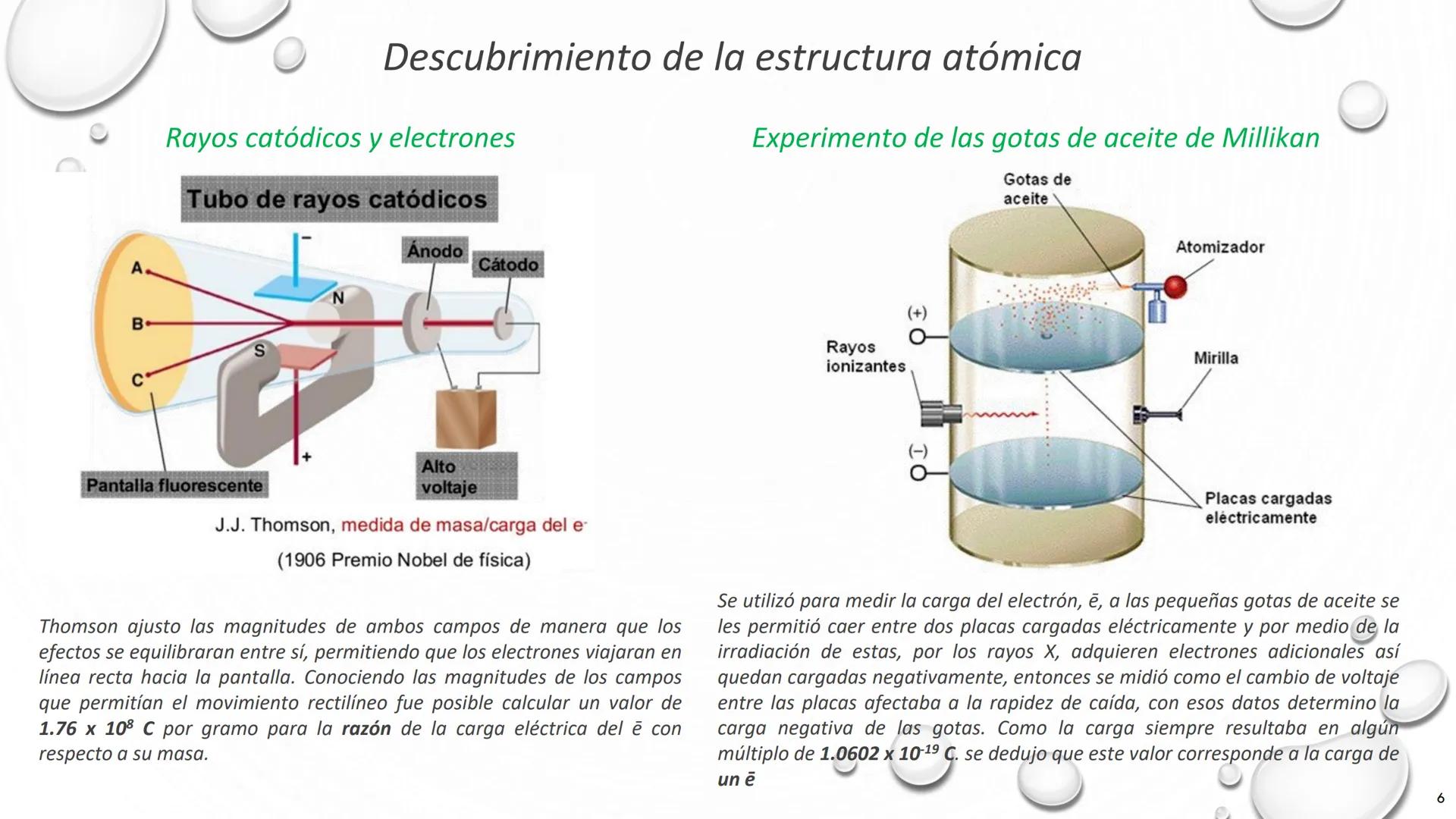
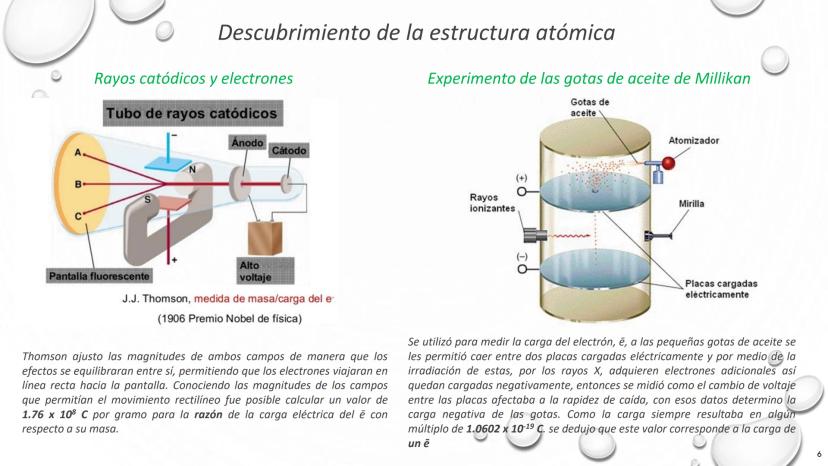
Los experimentos con rayos catódicos marcaron un punto de inflexión en nuestra comprensión del átomo. Estas investigaciones revelaron que los átomos no eran indivisibles como pensaba Dalton.
J.J. Thomson utilizó un tubo de rayos catódicos donde aplicó campos eléctricos y magnéticos para desviar partículas cargadas. Descubrió que estas partículas, los electrones, tenían una relación carga/masa constante de 1,76 x 10⁸ C/g. Este experimento revolucionario le valió el Premio Nobel de Física en 1906.
Posteriormente, Robert Millikan realizó su famoso experimento de la gota de aceite. Midió cómo pequeñas gotas de aceite cargadas eléctricamente caían entre dos placas con voltaje variable. Observó que la carga eléctrica siempre era un múltiplo de 1,602 x 10⁻¹⁹ C, identificando así la carga fundamental del electrón.
🔬 Estos experimentos fundamentales no solo demostraron la existencia de partículas subatómicas, sino que también proporcionaron las primeras mediciones precisas de sus propiedades físicas.
El descubrimiento del electrón fue el primer paso para comprender que los átomos tienen una estructura interna compleja, lo que llevó eventualmente a los modelos atómicos modernos.
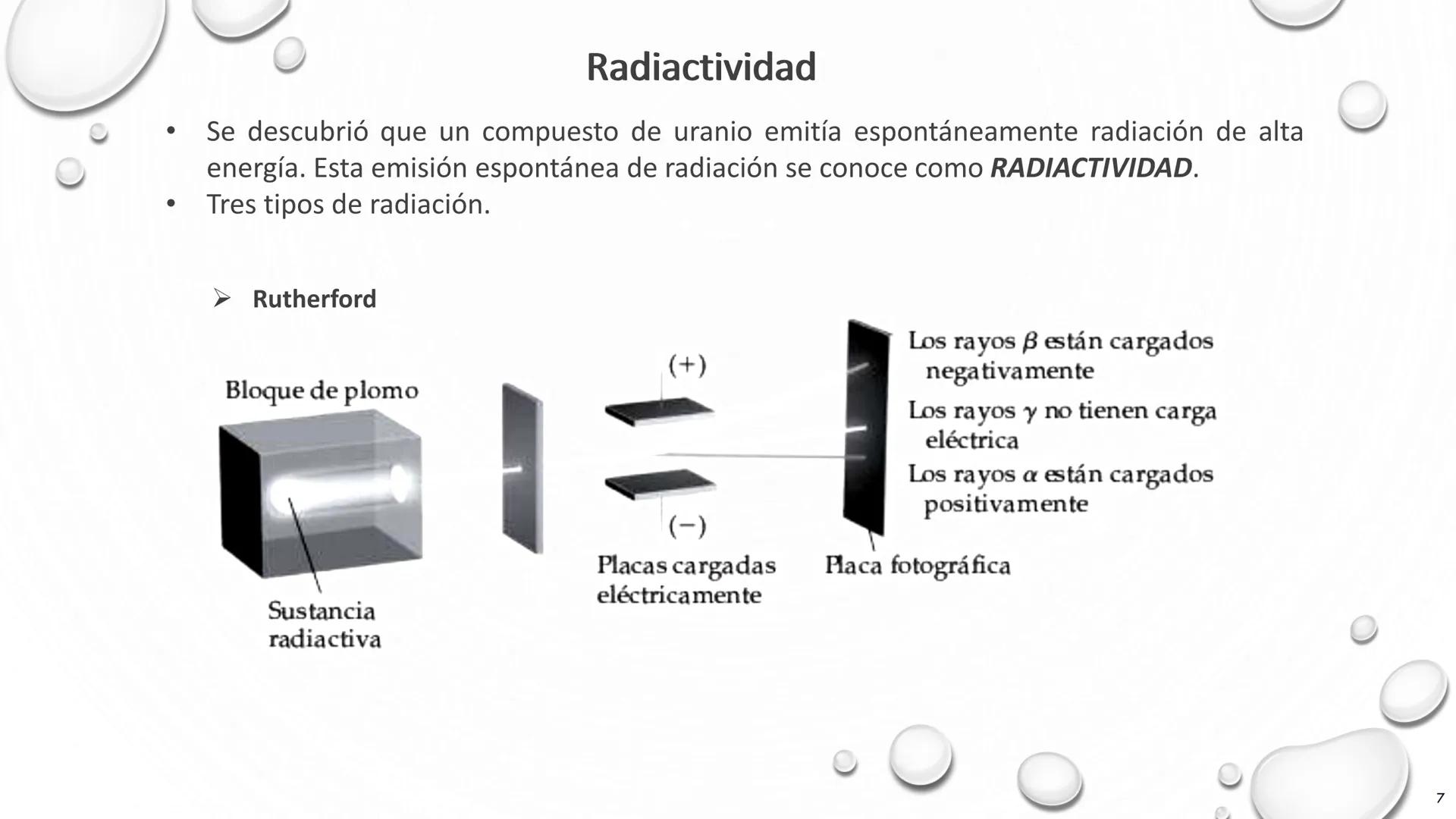
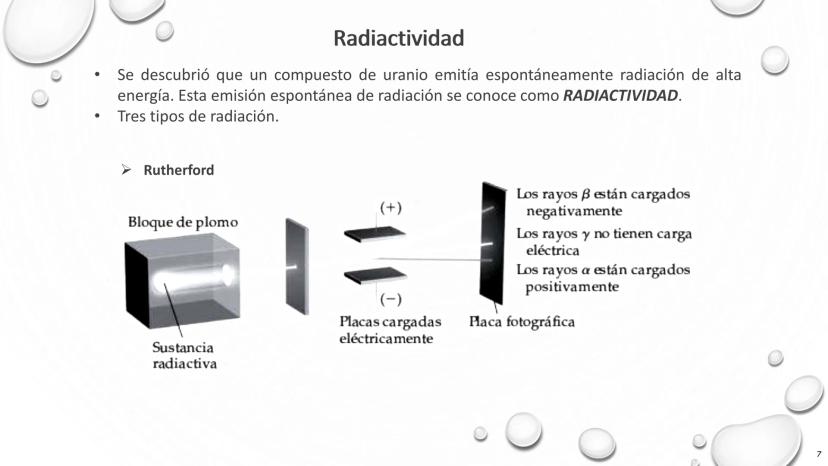
La radiactividad, descubierta inicialmente en compuestos de uranio, transformó nuestra comprensión del átomo revelando que algunos núcleos son inestables y emiten energía espontáneamente.
Rutherford investigó estos misteriosos rayos utilizando un ingenioso experimento. Colocó una sustancia radiactiva frente a placas cargadas eléctricamente y un bloque de plomo con una pequeña apertura, permitiendo que la radiación pasara hacia una placa fotográfica. Este diseño le permitió identificar tres tipos distintos de radiación:
💡 Este experimento fue crucial porque demostró que la radiactividad no era un fenómeno único, sino que consistía en diferentes tipos de emisiones con propiedades distintas.
La radiactividad no solo probó que los átomos pueden descomponerse (contradiciendo la teoría de Dalton), sino que también proporcionó herramientas para investigar la estructura nuclear del átomo.

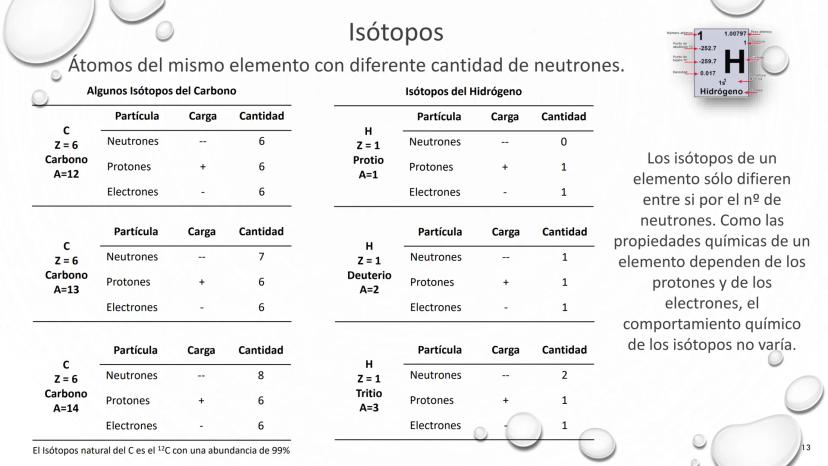
Los isótopos radiactivos han revolucionado la medicina moderna, permitiéndonos diagnosticar y tratar enfermedades que antes eran imposibles de detectar o curar.
Algunos isótopos tienen núcleos inestables con exceso de neutrones que se descomponen naturalmente, liberando energía que podemos aprovechar con fines médicos. Cada isótopo tiene propiedades únicas que lo hacen adecuado para usos específicos:
El Radio-226 fue uno de los primeros isótopos usados para tratar cáncer de piel, mientras que el Cobalto-60 emite radiación más potente y económica para tratar varios tipos de cáncer.
Para diagnóstico, el Tecnecio-99 es invaluable en la identificación de problemas óseos y bloqueos vasculares, mientras que el Yodo-131 se concentra naturalmente en la tiroides, permitiendo tratamientos precisos del cáncer tiroideo.
🏥 Los isótopos radiactivos actúan como pequeños "faros" dentro del cuerpo, permitiendo a los médicos ver y tratar problemas que serían invisibles con otras técnicas.
El Fósforo-32 tiene afinidad por los huesos y la médula ósea, haciéndolo ideal para diagnosticar enfermedades relacionadas con estos tejidos. Por su parte, el Arsénico-74 ayuda a detectar tumores cerebrales con precisión.
Esta aplicación pacífica de la física nuclear salva millones de vidas cada año.
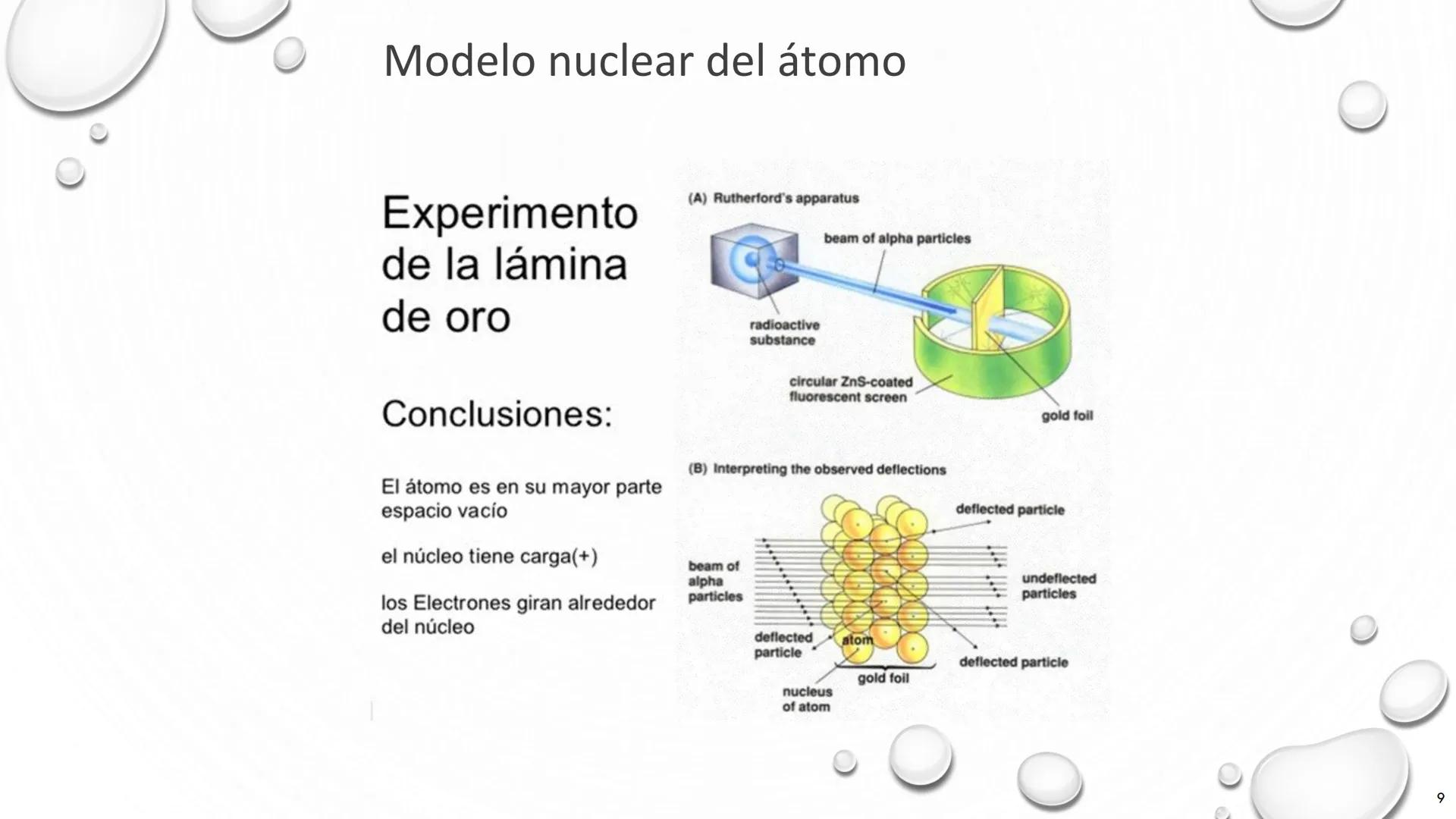
El famoso experimento de la lámina de oro de Rutherford transformó nuestra comprensión de la estructura atómica. Antes de este experimento, se creía que los átomos eran esferas sólidas con cargas positivas y negativas distribuidas uniformemente (modelo de Thomson).
En el experimento, Rutherford bombardeó una delgadísima lámina de oro con partículas alfa (núcleos de helio cargados positivamente). Esperaba que todas las partículas atravesaran la lámina con mínimas desviaciones, pero observó algo sorprendente:
Estas observaciones llevaron a tres conclusiones revolucionarias:
🔍 Este experimento fue tan inesperado que Rutherford lo comparó con "disparar un proyectil de 15 pulgadas contra un papel de seda y que rebote hacia ti".
El modelo nuclear sentó las bases para nuestra comprensión moderna del átomo, aunque todavía faltaba explicar la estabilidad de los electrones en órbita.
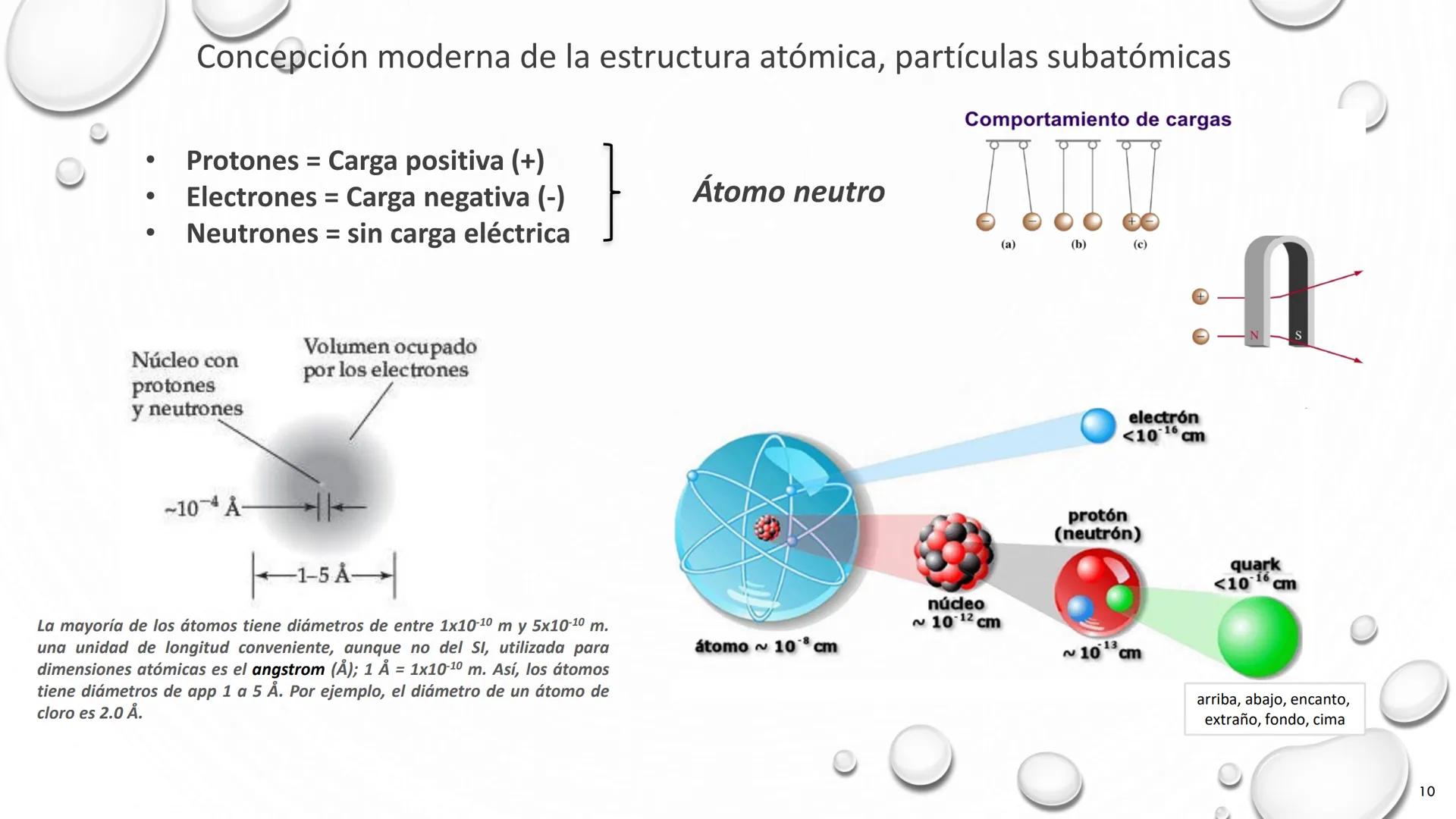
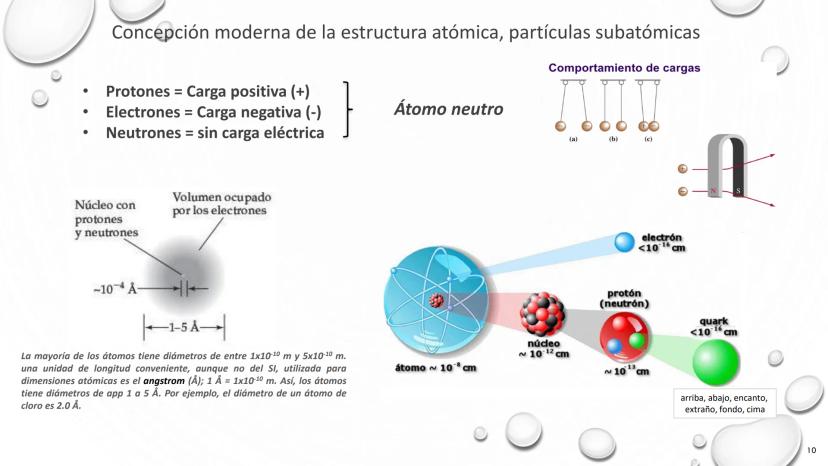
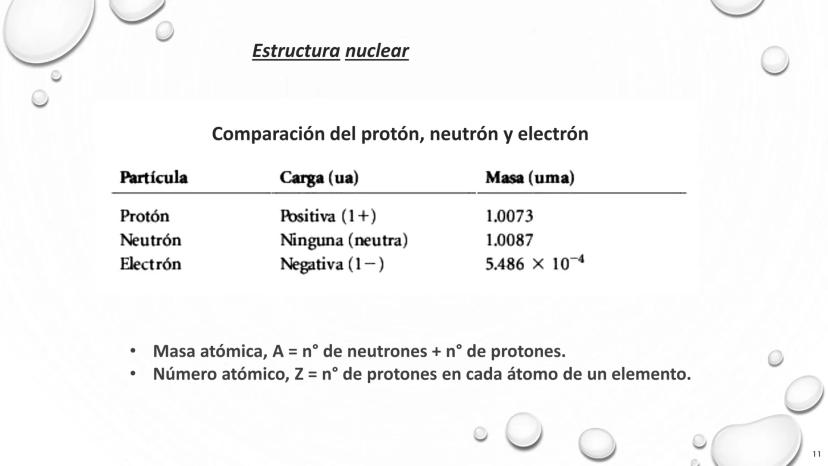
Nuestro modelo actual del átomo reconoce tres partículas subatómicas fundamentales: protones con carga positiva, electrones con carga negativa y neutrones sin carga eléctrica. Esta estructura explica tanto las propiedades químicas como físicas de la materia.
En un átomo neutro, el número de protones iguala exactamente al de electrones, equilibrando la carga eléctrica. Los protones y neutrones, con masas similares, se concentran en el núcleo increíblemente pequeño, mientras que los electrones, mucho más ligeros, ocupan el volumen restante.
Las dimensiones atómicas son fascinantes por su escala:
💫 Si un átomo fuera del tamaño de un estadio de fútbol, su núcleo sería como una canica en el centro. ¡El resto sería espacio prácticamente vacío!
Entender esta estructura nos permite predecir cómo se comportarán los átomos en reacciones químicas, cómo formarán moléculas y explicar propiedades fundamentales de la materia como conductividad, estado físico y reactividad.




Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
_2ogj9
@_2ogj9
La teoría atómica es el fundamento científico que explica cómo se estructura la materia a nivel microscópico. A través de los siglos, diferentes científicos han propuesto modelos cada vez más precisos para comprender el átomo, llevándonos desde las simples esferas... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La comprensión del átomo ha evolucionado dramáticamente desde el siglo XIX hasta la actualidad. Esta línea de tiempo representa el desarrollo de los modelos atómicos, mostrando cómo nuestro entendimiento de la materia ha pasado por varias transformaciones fundamentales.
En 1803, Dalton propuso que toda materia está compuesta por partículas indivisibles. Para 1897, Thomson descubrió el electrón, cambiando completamente nuestra visión. Luego, en 1909, Rutherford identificó el núcleo atómico, y en 1913, Bohr introdujo la idea de niveles energéticos específicos para los electrones.
💡 Cada modelo atómico no simplemente reemplazó al anterior, sino que incorporó las observaciones anteriores y añadió nuevas capas de entendimiento sobre la estructura fundamental de la materia.
El modelo actual es el resultado de siglos de investigación científica y nos permite explicar prácticamente todos los fenómenos químicos y físicos relacionados con la materia.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La evolución de los modelos atómicos representa uno de los mayores avances científicos. Cada modelo nos ha acercado a entender la verdadera naturaleza de la materia.
Dalton (1803-1807) propuso que todos los elementos están formados por átomos indivisibles, como pequeñas esferas sólidas. Este modelo simple sentó las bases para el desarrollo posterior.
Thomson (1904) propuso el modelo del "pudín con pasas", donde los electrones negativos estaban incrustados en una masa positiva, como pasas en un pudín.
Rutherford (1911) descubrió que el átomo tiene un núcleo central donde se concentra la carga positiva, con electrones girando alrededor, similar al sistema solar.
Bohr (1913) introdujo los niveles de energía, estableciendo que los electrones orbitan el núcleo en niveles fijos y específicos.
Schrödinger (1926) revolucionó nuestra comprensión con el modelo de nube de electrones y orbitales, basado en la mecánica cuántica y probabilidades.
El modelo atómico actual combina aspectos de todos los anteriores, pero se basa principalmente en la teoría cuántica, describiendo los electrones como nubes de probabilidad en lugar de partículas con posiciones exactas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La teoría de Dalton (1803-1807) fue revolucionaria al proponer que toda materia está formada por unidades fundamentales indivisibles. Sus cuatro postulados principales siguen siendo relevantes en la química básica.
Los elementos están formados por partículas diminutas llamadas átomos. Estas partículas son tan pequeñas que no podían verse con la tecnología de la época, pero Dalton dedujo su existencia mediante observaciones indirectas.
Los átomos de un mismo elemento son idénticos entre sí, pero diferentes a los de otros elementos. Por ejemplo, todos los átomos de oxígeno son iguales entre sí, pero distintos a los átomos de nitrógeno.
Los átomos son indestructibles y no se transforman durante las reacciones químicas. Este principio establece que los átomos no se crean ni se destruyen, solo se reorganizan.
Los compuestos se forman cuando átomos de diferentes elementos se combinan en proporciones fijas. Por ejemplo, el óxido nítrico (NO) siempre contiene un átomo de nitrógeno y uno de oxígeno.
🔍 Aunque algunos aspectos de la teoría de Dalton han sido modificados con el tiempo (ahora sabemos que los átomos son divisibles), sus ideas fundamentales sobre la conservación de la materia y las proporciones constantes siguen siendo pilares de la química moderna.
Esta teoría permitió explicar muchas observaciones experimentales y sentó las bases para el desarrollo de la química moderna.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La teoría atómica de Dalton no surgió de la nada, sino que explicaba elegantemente varias leyes químicas que ya habían sido observadas experimentalmente.
La ley de la composición constante afirma que un compuesto específico siempre contiene los mismos elementos en las mismas proporciones. Por ejemplo, el agua siempre tiene dos átomos de hidrógeno por cada átomo de oxígeno, independientemente de su origen.
La ley de conservación de la masa establece que la masa total antes y después de una reacción química permanece constante. Esto tiene sentido con la teoría de Dalton, ya que los átomos no se crean ni se destruyen, solo se reorganizan.
La ley de las proporciones múltiples dice que cuando dos elementos forman más de un compuesto, las masas de un elemento que se combinan con una masa fija del otro están en relación de números enteros pequeños. Esta ley fue crucial para demostrar la naturaleza atómica de la materia.
Estas leyes proporcionaron evidencia sólida para la teoría atómica, permitiendo a los científicos predecir el comportamiento químico incluso antes de poder observar directamente los átomos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Te has preguntado cómo podemos demostrar la ley de las proporciones múltiples? El agua (H₂O) y el peróxido de hidrógeno (H₂O₂) nos ofrecen un ejemplo perfecto.
Ambos compuestos contienen los mismos elementos (hidrógeno y oxígeno), pero en proporciones diferentes. Al analizar 1 gramo de hidrógeno en cada compuesto:
| Elemento | H₂O | H₂O₂ |
|---|---|---|
| H | 1.0g | 1.0g |
| O | 8.0g | 16.0g |
La relación entre las masas de oxígeno es exactamente 1:2, un número entero simple. Este patrón no es coincidencia, sino evidencia directa de que la materia está compuesta por átomos que se combinan en proporciones fijas.
💡 La razón por la que obtenemos números enteros simples es porque estamos contando átomos, aunque indirectamente a través de sus masas.
Este fenómeno se observa constantemente en todos los compuestos químicos y proporciona una de las evidencias más convincentes de la naturaleza atómica de la materia, confirmando la brillante intuición de Dalton hace más de 200 años.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los experimentos con rayos catódicos marcaron un punto de inflexión en nuestra comprensión del átomo. Estas investigaciones revelaron que los átomos no eran indivisibles como pensaba Dalton.
J.J. Thomson utilizó un tubo de rayos catódicos donde aplicó campos eléctricos y magnéticos para desviar partículas cargadas. Descubrió que estas partículas, los electrones, tenían una relación carga/masa constante de 1,76 x 10⁸ C/g. Este experimento revolucionario le valió el Premio Nobel de Física en 1906.
Posteriormente, Robert Millikan realizó su famoso experimento de la gota de aceite. Midió cómo pequeñas gotas de aceite cargadas eléctricamente caían entre dos placas con voltaje variable. Observó que la carga eléctrica siempre era un múltiplo de 1,602 x 10⁻¹⁹ C, identificando así la carga fundamental del electrón.
🔬 Estos experimentos fundamentales no solo demostraron la existencia de partículas subatómicas, sino que también proporcionaron las primeras mediciones precisas de sus propiedades físicas.
El descubrimiento del electrón fue el primer paso para comprender que los átomos tienen una estructura interna compleja, lo que llevó eventualmente a los modelos atómicos modernos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La radiactividad, descubierta inicialmente en compuestos de uranio, transformó nuestra comprensión del átomo revelando que algunos núcleos son inestables y emiten energía espontáneamente.
Rutherford investigó estos misteriosos rayos utilizando un ingenioso experimento. Colocó una sustancia radiactiva frente a placas cargadas eléctricamente y un bloque de plomo con una pequeña apertura, permitiendo que la radiación pasara hacia una placa fotográfica. Este diseño le permitió identificar tres tipos distintos de radiación:
💡 Este experimento fue crucial porque demostró que la radiactividad no era un fenómeno único, sino que consistía en diferentes tipos de emisiones con propiedades distintas.
La radiactividad no solo probó que los átomos pueden descomponerse (contradiciendo la teoría de Dalton), sino que también proporcionó herramientas para investigar la estructura nuclear del átomo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los isótopos radiactivos han revolucionado la medicina moderna, permitiéndonos diagnosticar y tratar enfermedades que antes eran imposibles de detectar o curar.
Algunos isótopos tienen núcleos inestables con exceso de neutrones que se descomponen naturalmente, liberando energía que podemos aprovechar con fines médicos. Cada isótopo tiene propiedades únicas que lo hacen adecuado para usos específicos:
El Radio-226 fue uno de los primeros isótopos usados para tratar cáncer de piel, mientras que el Cobalto-60 emite radiación más potente y económica para tratar varios tipos de cáncer.
Para diagnóstico, el Tecnecio-99 es invaluable en la identificación de problemas óseos y bloqueos vasculares, mientras que el Yodo-131 se concentra naturalmente en la tiroides, permitiendo tratamientos precisos del cáncer tiroideo.
🏥 Los isótopos radiactivos actúan como pequeños "faros" dentro del cuerpo, permitiendo a los médicos ver y tratar problemas que serían invisibles con otras técnicas.
El Fósforo-32 tiene afinidad por los huesos y la médula ósea, haciéndolo ideal para diagnosticar enfermedades relacionadas con estos tejidos. Por su parte, el Arsénico-74 ayuda a detectar tumores cerebrales con precisión.
Esta aplicación pacífica de la física nuclear salva millones de vidas cada año.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El famoso experimento de la lámina de oro de Rutherford transformó nuestra comprensión de la estructura atómica. Antes de este experimento, se creía que los átomos eran esferas sólidas con cargas positivas y negativas distribuidas uniformemente (modelo de Thomson).
En el experimento, Rutherford bombardeó una delgadísima lámina de oro con partículas alfa (núcleos de helio cargados positivamente). Esperaba que todas las partículas atravesaran la lámina con mínimas desviaciones, pero observó algo sorprendente:
Estas observaciones llevaron a tres conclusiones revolucionarias:
🔍 Este experimento fue tan inesperado que Rutherford lo comparó con "disparar un proyectil de 15 pulgadas contra un papel de seda y que rebote hacia ti".
El modelo nuclear sentó las bases para nuestra comprensión moderna del átomo, aunque todavía faltaba explicar la estabilidad de los electrones en órbita.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro modelo actual del átomo reconoce tres partículas subatómicas fundamentales: protones con carga positiva, electrones con carga negativa y neutrones sin carga eléctrica. Esta estructura explica tanto las propiedades químicas como físicas de la materia.
En un átomo neutro, el número de protones iguala exactamente al de electrones, equilibrando la carga eléctrica. Los protones y neutrones, con masas similares, se concentran en el núcleo increíblemente pequeño, mientras que los electrones, mucho más ligeros, ocupan el volumen restante.
Las dimensiones atómicas son fascinantes por su escala:
💫 Si un átomo fuera del tamaño de un estadio de fútbol, su núcleo sería como una canica en el centro. ¡El resto sería espacio prácticamente vacío!
Entender esta estructura nos permite predecir cómo se comportarán los átomos en reacciones químicas, cómo formarán moléculas y explicar propiedades fundamentales de la materia como conductividad, estado físico y reactividad.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
1
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas de Estudio Interactivas ✓ Prueba Completa de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia